题目内容
13. 在探究空气中氧气的体积含量测定实验中,要注意观察实验现象,体会从实验事实导出结论的思维过程(如图1).某同学实验中观察到,红磷燃烧,产生大量的白烟,放出大量热;打开弹簧夹后,烧杯中的水沿导气管进入集气瓶,结果占集气瓶内空间的水少于$\frac{1}{5}$.他再次实验,结果占集气瓶内空间的水多于$\frac{1}{5}$
在探究空气中氧气的体积含量测定实验中,要注意观察实验现象,体会从实验事实导出结论的思维过程(如图1).某同学实验中观察到,红磷燃烧,产生大量的白烟,放出大量热;打开弹簧夹后,烧杯中的水沿导气管进入集气瓶,结果占集气瓶内空间的水少于$\frac{1}{5}$.他再次实验,结果占集气瓶内空间的水多于$\frac{1}{5}$请你帮他找找实验失败原因:
少于$\frac{1}{5}$:红磷的量不足;装置漏气;未等装置冷却到常温即打开止水夹;
多于$\frac{1}{5}$:在将燃着的红磷伸入装置时动作缓慢,致使装置内的部分空气逸散出来.
分析 本题是用红磷测定空气中氧气的含量,本探究实验一般要注意以下几点:①装置的气密性好;②所用药品红磷的量,必须是足量;③读数时一定要冷却到原温度;④生成物的状态一般要求是固态等.如果控制不好条件,进入集气瓶中水体积会小于五分之一.如果装置内的部分空气逸散出来,就会导致进入集气瓶中水体积大于五分之一.
解答 解:本题中进入集气瓶中水的体积小于五分之一,有可能有以下几点:装置漏气、红磷的量不足、没有冷却就读数;如果进入集气瓶中水的体积大于五分之一,就说明操作太慢,致使装置内的部分空气逸散出来.故答案为:红磷的量不足;装置漏气;未等装置冷却到常温即打开止水夹.
在将燃着的红磷伸入装置时动作缓慢,致使装置内的部分空气逸散出来.
点评 本考点是测定氧气在空气中的体积分数,属于与课本知识同类信息.本探究实验在不同版本的教材中用的实验装置是不一样的,不论用哪一套装置,其原理是一致的,问题也是大同小异,就是为了证明氧气约占空气体积的五分之一的.希望同学们认真把握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8. 一只盛有稀硫酸的烧杯中,漂浮着一块木块(如图),往烧杯加入适量某种固体物质后,木块浸没在水中的体积变小(假设此过程中溶液的体积变 化忽略不计),加入的固体物质可能是( )
一只盛有稀硫酸的烧杯中,漂浮着一块木块(如图),往烧杯加入适量某种固体物质后,木块浸没在水中的体积变小(假设此过程中溶液的体积变 化忽略不计),加入的固体物质可能是( )
 一只盛有稀硫酸的烧杯中,漂浮着一块木块(如图),往烧杯加入适量某种固体物质后,木块浸没在水中的体积变小(假设此过程中溶液的体积变 化忽略不计),加入的固体物质可能是( )
一只盛有稀硫酸的烧杯中,漂浮着一块木块(如图),往烧杯加入适量某种固体物质后,木块浸没在水中的体积变小(假设此过程中溶液的体积变 化忽略不计),加入的固体物质可能是( )| A. | Ba(OH)2 | B. | Cu | C. | Fe | D. | BaCl2 |
18.下列化学方程式正确的是( )
| A. | Mg+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$ MgSO4+H2 | |
| B. | 2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | |
| C. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$ 2P2O5 | |
| D. | 2NaNO3+K2CO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2KNO3+Na2CO3 |
3.根据实验操作填表:
| 实验 | 现象 |
| 澄清石灰水中滴加酚酞溶液 | |
| 碳酸钠粉末与稀盐酸反应 |

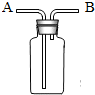 如图所示装置有多种用途,请回答下列问题:
如图所示装置有多种用途,请回答下列问题: