题目内容
将Cu与CuO和混合物放入足量的稀盐酸中,充分反应后过滤,洗净,干燥,则滤纸上的物质是 ,写出发生反应的化学方程式 .
【答案】分析:根据铜不与盐酸反应,氧化铜能与稀盐酸反应以及化学方程式的书写规则进行回答.
解答:解:铜不与盐酸反应,氧化铜能与稀盐酸反应,故充分反应后,滤纸上的物质是未反应的铜,氧化铜与稀盐酸反应生成了氯化铜和水,
反应的化学方程式为:CuO+2HCl═CuCl2+H2O
故答案为:Cu;CuO+2HCl═CuCl2+H2O;
点评:本题考查了酸的化学性质,排在氢后面的金属不能与酸反应.
解答:解:铜不与盐酸反应,氧化铜能与稀盐酸反应,故充分反应后,滤纸上的物质是未反应的铜,氧化铜与稀盐酸反应生成了氯化铜和水,
反应的化学方程式为:CuO+2HCl═CuCl2+H2O
故答案为:Cu;CuO+2HCl═CuCl2+H2O;
点评:本题考查了酸的化学性质,排在氢后面的金属不能与酸反应.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
为测定H2SO4和CuSO4的混合溶液中溶质的含量,小强和小国设计并进行了以下实验.
【查阅资料】①Cu(OH)2固体受热易分解产生CuO和H2O;②BaSO4固体受热难分解.
【实验一】目的:测定100.0g混合溶液中CuSO4的质量
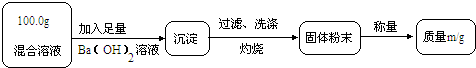
(1)小强认为m1是CuO的质量,小国提出质疑,认为m1是 的质量.
(2)为得到CuO的质量,小国决定将Ba(OH)2溶液换成另一种溶液,该溶液可以是 (填字母).
A.NaOH溶液、B.KOH溶液、C.BaCl2溶液
(3)改进实验后小国得到8.0g CuO,试求100.0g混合溶液中CuSO4的质量.
解:
【实验二】目的:测定100.0 g混合溶液中H2SO4的质量分数
主要实验步骤如下: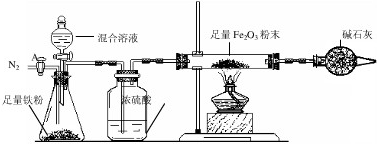
a.按图组装仪器,检查气密性,装好药品,其中Fe2O3的质量为m2g;
b.打开活塞A,通入N2一段时间,关闭活塞A;
c.点燃酒精灯,逐滴加入100.0g混合溶液;
d.测定反应过程中硬质玻璃管内物质的质量(见表格所示);
e.待反应结束后,熄灭酒精灯,打开活塞A,缓缓通一会儿N2.
记录数据
过滤、洗涤干燥、称量
(4)请结合以上实验数据(假设与Fe2O3反应的气体的损耗忽略),计算100.0g混合溶液中H2SO4的质量分数为 .(可能用到的相对分子质量:Fe2O3-160,H2SO4-98)
【查阅资料】①Cu(OH)2固体受热易分解产生CuO和H2O;②BaSO4固体受热难分解.
【实验一】目的:测定100.0g混合溶液中CuSO4的质量

(1)小强认为m1是CuO的质量,小国提出质疑,认为m1是
(2)为得到CuO的质量,小国决定将Ba(OH)2溶液换成另一种溶液,该溶液可以是
A.NaOH溶液、B.KOH溶液、C.BaCl2溶液
(3)改进实验后小国得到8.0g CuO,试求100.0g混合溶液中CuSO4的质量.
解:
【实验二】目的:测定100.0 g混合溶液中H2SO4的质量分数
主要实验步骤如下:

a.按图组装仪器,检查气密性,装好药品,其中Fe2O3的质量为m2g;
b.打开活塞A,通入N2一段时间,关闭活塞A;
c.点燃酒精灯,逐滴加入100.0g混合溶液;
d.测定反应过程中硬质玻璃管内物质的质量(见表格所示);
e.待反应结束后,熄灭酒精灯,打开活塞A,缓缓通一会儿N2.
记录数据
| 时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
| 质量/g | m2 | m2-1.6 | m2-3.0 | m2-4.0 | m2-4.8 | m2-4.8 |
(4)请结合以上实验数据(假设与Fe2O3反应的气体的损耗忽略),计算100.0g混合溶液中H2SO4的质量分数为
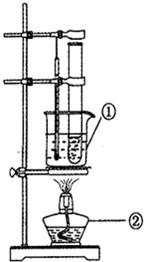 某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.
某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.
