题目内容
化学是一门以实验为基础的科学.

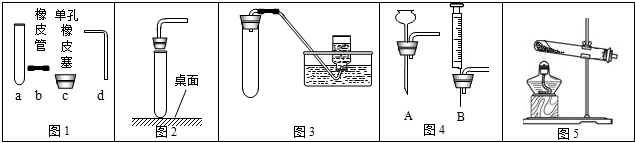
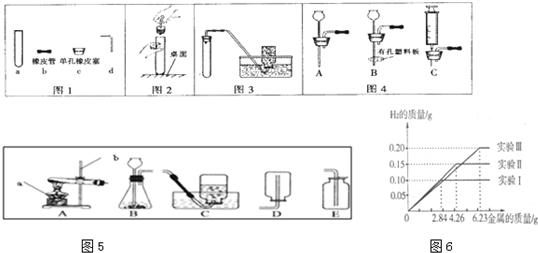
(1)根据图1回答:写出a的名称______;在连接c和d时,使d较易插入c中的措施是______.
(2)采用图2所示操作可能造成的后果之一是______.
(3)利用图3装置(夹持装置未画出)能进行的下列实验是______(填字母);
A用高锰酸钾制氧气 B用石灰石与稀盐酸制二氧化碳
C用锌与稀硫酸制氢气 D用双氧水与二氧化锰制氧气
写出你所选全部答案的化学方程式____________;若将图3中的水改为热水,上述选项中还可以可以增加一个答案______(填字母),理由是______.
(4)图3中的气体发生装置虽然简单,操作方便,但无法控制反应速率.请从图4中选取______(填字母)只作一处改进,即可与图1中a组装成新的气体发生装置,以达到控制反应速率的目的,你改进的方法是______.
解:(1)a仪器是试管,使d较易插入c中的措施是沾水湿润,目的是起到润滑作用;
(2)图二这样塞入容易压碎试管,或者导管断裂刺破手掌,正确的做法是先将橡皮塞润湿,左手拿试管,右手缓慢把其旋入;
(3)图三装置中的发生装置是固液制气装置的简易型式,反应不需要加热,可用于制取二氧化碳、氧气、氢气.但是收集装置是排水法,二氧化碳能溶于水,不能用来收集二氧化碳.故选CD;锌与稀硫酸反应生成硫酸锌和氢气,方程式是Zn+H2SO4═ZnSO4+H2↑,双氧水在二氧化锰的催化作用下生成水和氧气,方程式是2H2O2 2H2O+O2↑;由于气体的溶解度随温度的升高而减小,所以若将图3中的水改为热水,还可用来制取二氧化碳;
2H2O+O2↑;由于气体的溶解度随温度的升高而减小,所以若将图3中的水改为热水,还可用来制取二氧化碳;
(4)想控制反应速率就得控制反应物的量,图3中的气体发生装置虽然简单,操作方便,但无法控制反应速率,可从图4中选取B,图B虽能控制反应的进行但无法控制反应的速率,而分液漏斗可以控制液体的滴加速度,从而达到控制反应速率的目的,所以可将B中长颈漏斗换为分液漏斗即可达到控制反应速率的目的;
故答案为:(1)试管; 将插入橡皮管的导管一端用水湿润;
(2)试管底部破损(或刺破手);
(3)C、D;2H2O2 2H2O+O2↑; Zn+H2SO4═ZnSO4+H2↑;B; 温度升高,气体在水中的溶解度减小;
2H2O+O2↑; Zn+H2SO4═ZnSO4+H2↑;B; 温度升高,气体在水中的溶解度减小;
(4)B;将长颈漏斗改为分液漏斗.
分析:(1)据常用仪器分析,使d较易插入c中的措施是沾水湿润,目的是起到润滑作用;
(2)图二这样塞入容易压碎试管,或者导管断裂刺破手掌,正确的做法是先将橡皮塞润湿,左手拿试管,右手缓慢把其旋入;
(3)图三装置是固液制气装置的简易型式,可用于制取二氧化碳、氧气、氢气,然后据反应原理书写方程式,气体的溶解度随温度的升高而减小;
(4)想控制反应速率就得控制反应物的量,据此结合仪器的作用分析解答.
点评:解答时要注意:玻璃仪器连接时一般要先湿润润滑,初中化学中典型的固液制气主要有制取二氧化碳、氢气、氧气(双氧水于二氧化锰),并能正确书写反应方程式,同时明确仪器的用途和气体的溶解度受温度影响情况也是解答的关键因素.
(2)图二这样塞入容易压碎试管,或者导管断裂刺破手掌,正确的做法是先将橡皮塞润湿,左手拿试管,右手缓慢把其旋入;
(3)图三装置中的发生装置是固液制气装置的简易型式,反应不需要加热,可用于制取二氧化碳、氧气、氢气.但是收集装置是排水法,二氧化碳能溶于水,不能用来收集二氧化碳.故选CD;锌与稀硫酸反应生成硫酸锌和氢气,方程式是Zn+H2SO4═ZnSO4+H2↑,双氧水在二氧化锰的催化作用下生成水和氧气,方程式是2H2O2
 2H2O+O2↑;由于气体的溶解度随温度的升高而减小,所以若将图3中的水改为热水,还可用来制取二氧化碳;
2H2O+O2↑;由于气体的溶解度随温度的升高而减小,所以若将图3中的水改为热水,还可用来制取二氧化碳;(4)想控制反应速率就得控制反应物的量,图3中的气体发生装置虽然简单,操作方便,但无法控制反应速率,可从图4中选取B,图B虽能控制反应的进行但无法控制反应的速率,而分液漏斗可以控制液体的滴加速度,从而达到控制反应速率的目的,所以可将B中长颈漏斗换为分液漏斗即可达到控制反应速率的目的;
故答案为:(1)试管; 将插入橡皮管的导管一端用水湿润;
(2)试管底部破损(或刺破手);
(3)C、D;2H2O2
 2H2O+O2↑; Zn+H2SO4═ZnSO4+H2↑;B; 温度升高,气体在水中的溶解度减小;
2H2O+O2↑; Zn+H2SO4═ZnSO4+H2↑;B; 温度升高,气体在水中的溶解度减小;(4)B;将长颈漏斗改为分液漏斗.
分析:(1)据常用仪器分析,使d较易插入c中的措施是沾水湿润,目的是起到润滑作用;
(2)图二这样塞入容易压碎试管,或者导管断裂刺破手掌,正确的做法是先将橡皮塞润湿,左手拿试管,右手缓慢把其旋入;
(3)图三装置是固液制气装置的简易型式,可用于制取二氧化碳、氧气、氢气,然后据反应原理书写方程式,气体的溶解度随温度的升高而减小;
(4)想控制反应速率就得控制反应物的量,据此结合仪器的作用分析解答.
点评:解答时要注意:玻璃仪器连接时一般要先湿润润滑,初中化学中典型的固液制气主要有制取二氧化碳、氢气、氧气(双氧水于二氧化锰),并能正确书写反应方程式,同时明确仪器的用途和气体的溶解度受温度影响情况也是解答的关键因素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
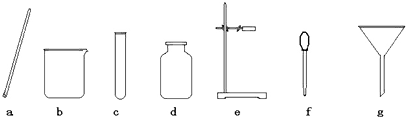
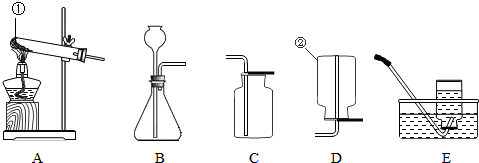
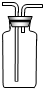
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: