题目内容
下列现象不能用质量守恒定律解释的是
A.将2g氢气在16g氧气中燃烧,生成18g水
B.将20ml酒精与20ml水混合,总体积小于40ml.
C.镁条燃烧后的质量比镁条质量大
D.蜡烛燃烧后质量变轻了
B
【解析】
试题分析:质量守恒定律是指在化学反应中参与反应的反应物总质量等生成物的总质量。A、是化学反应且质量相等;B、物理变化且计算的是体积,不符合;C、镁条燃烧是指镁和氧气反应生成氧化镁,即m(Mg)+m(O2)=(MgO),那么燃烧后产物氧化镁质量当然比镁更重,可以用质量守恒定律解释;D、蜡烛燃烧是指蜡烛和氧气反应生成水(气体)和二氧化碳(气体),m(蜡烛)+m(O2)=m(H2O)+m(CO2),产物是气体都逸走了,质量变轻。
考点:质量守恒定律

练习册系列答案
相关题目
科学探究中常用到推理的方法。根据下列实验事实推出的结论正确的是
编号 | 事实 | 结论 |
A | 水能灭火 | 所有物质着火都能用水熄灭 |
B | 点燃氢气生成水;电解水生成氢气和氧气 | 两个实验都证明水是由氢氧两种元素组成 |
C | 化合物由不同元素组成 | 含有不同元素的物质一定是化合物 |
D | 镁条在空气中燃烧,质量减轻 | 该反应不遵守质量守恒定律 |

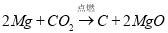 ,以下说法不正确的是
,以下说法不正确的是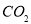 灭火器进行灭火
灭火器进行灭火