题目内容
12.下列物质间发生的化学反应属于中和反应的是( )| A. | Zn+HCl | B. | H2SO4+NaOH | C. | CuO+HCl | D. | HCl+AgNO3 |
分析 中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐和水,据此进行分析判断.
解答 解:A、锌与稀盐酸反应生成氯化锌和氢气,反应物是金属和酸,不是酸与碱的反应,不属于中和反应,故选项错误.
B、硫酸与氢氧化钠反应生成硫酸钠和水,反应物是酸和碱,生成物是盐和水,属于中和反应,故选项正确.
C、氧化铜与盐酸反应生成氯化铜和水,反应物是金属氧化物和酸,不是酸与碱的反应,不属于中和反应,故选项错误.
D、盐酸与硝酸银溶液反应生成氯化银沉淀和硝酸,反应物是酸和盐,不是酸与碱的反应,不属于中和反应,故选项错误.
故选:B.
点评 本题难度不大,掌握中和反应的特征(反应物是酸和碱,生成物是盐和水)是正确解答此类题的关键.

练习册系列答案
相关题目
2.下列关于物质性质或实验现象的描述错误的是( )
| A. | 红磷在氧气中燃烧,产生大量白烟 | |
| B. | 铁丝在氧气中燃烧,火星四射,生出一种黑色固体 | |
| C. | 铁锈和稀硫酸反应生成硫酸亚铁和氢气 | |
| D. | 打开盛有浓盐酸试剂瓶的瓶塞,瓶口有白雾产生 |
3. 根据如表提供的信息,下列判断正确的是( )
根据如表提供的信息,下列判断正确的是( )
 根据如表提供的信息,下列判断正确的是( )
根据如表提供的信息,下列判断正确的是( )| A. | 钠离子核外有三个电子层 | |
| B. | 元素所在的周期数等于其原子的电子层数 | |
| C. | 第二、三周期元素的原子从左至右最外层电子数逐渐减少 | |
| D. | 在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2 |
20.物质的制取、除杂、检验和鉴别时化学实验的重要内容,下列实验方案设计能够达到目的是( )
| 选项 | 实验内容 | 实验方案设计 |
| A | 制取少量纯净的氢气 | 选用金属镁和浓盐酸反应,直接收集即可 |
| B | 除去粗盐中混有的Na2SO4 | 加入过量Ba(NO3)2溶液,过滤 |
| C | 检验实验室制取CO2的剩余废液中仍含有盐酸 | 加适量AgNO3溶液,产生白色沉淀即可证明 |
| D | 鉴别石灰水和氢氧化钠溶液 | 分别滴加Na2CO3溶液,变白色浑浊的是石灰水 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
7.下列各组离子能大量共存于某pH=2的无色溶液中的是( )
| A. | K+、OH-、NO3- | B. | Cu2+、Cl-、NH4+ | C. | Ca2+、Cl-、CO32- | D. | Na+、K+、SO42- |
4.建立基本的化学观念可以让我们更好地理解化学,如形成守恒观念,可以更好地理解质量守恒定律.下列表述正确的是( )
| A. | 1个C原子和1个O2分子反应,生成2个CO2分子 | |
| B. | 32 g S与32 g O2完全反应,生成64 g SO2 | |
| C. | 镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律 | |
| D. | 根据:蜡烛+氧气$\stackrel{点燃}{→}$二氧化碳+水,则蜡烛中一定含有C、H、O三种元素 |
1.下列各组物间的转化,在一定条件下均能一步实现的一组是( )
| A. | Fe→Fe2O3→FeCl2 | B. | CaCO3→CO2→CO | ||
| C. | CuO→Cu (OH)2→CuSO4 | D. | HNO3→NaNO3→NaCl |

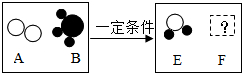

 表示氢原子,用
表示氢原子,用 表示氧原子);你补充C图的依据是
表示氧原子);你补充C图的依据是 .
.