题目内容
14.现有Ca、O、C、H四种元素中,请选用其中一种或几种元素写出符合下列要求的化学式各写一个:(1)最理想的燃料H2;
(2)空气中体积分数占第二位的气体O2;
(3)切割玻璃C;
(4)西气东输的主要气体CH4;
(5)汽水中含有的不稳定的酸H2CO3;
(6)大理石的主要成分CaCO3.
分析 首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)氢气燃烧称为是水,无污染,是最理想的燃料,其化学式为:H2.故填:H2;
(2)空气中体积分数占第二位的气体是氧气,其化学式为:O2.故填:O2;
(3)金刚石的硬度很大,可用来切割玻璃,故填:C;
(4)西气东输的气体是天然气,其主要成分是甲烷,故填:CH4;
(5)汽水中含有不稳定酸是碳酸,故填:H2CO3;
(6)大理石的主要成分是碳酸钙,故填:CaCO3
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在;解题时应注意只能从给出的元素中选择来组成物质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.某同学欲测定大理石中碳酸钙的质量分数,称取12.5g大理石与100g稀盐酸恰好反应(假设杂质不与盐酸反应,忽略盐酸的挥发),数据如表:
根据实验数据回答下列问题:
(1)当反应时间为t1时,对应的气体质量m为0.8g.
(2)通过化学方程式计算大理石中碳酸钙的质量分数.
(3)所用盐酸的质量分数是多少?
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/s | 0 | 0.8 | 1.1 | 2.2 | 4.4 | 4.4 | n |
(1)当反应时间为t1时,对应的气体质量m为0.8g.
(2)通过化学方程式计算大理石中碳酸钙的质量分数.
(3)所用盐酸的质量分数是多少?
19.下列对实验现象的描述或实验操作正确的是( )
| A. | 红磷在氧气中燃烧,生成浓重的白雾 | |
| B. | 进行一氧化碳还原氧化铁实验,实验前必须检验其纯度 | |
| C. | 用氢氧化钠固体与稀盐酸作用,验证得出中和反应放热 | |
| D. | 稀释浓硫酸时,将水倒入浓硫酸中,并不断搅拌 |
3.下列物质由离子直接构成的是( )
| A. | 氯化氢 | B. | 石墨 | C. | 氯化镁 | D. | 氮气 |
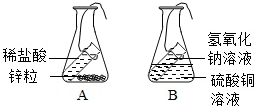 小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究.请填写以下探究过程中的空格:
小洁以“化学反应中,反应物与生成物的质量关系”为课题进行科学探究.请填写以下探究过程中的空格: