题目内容
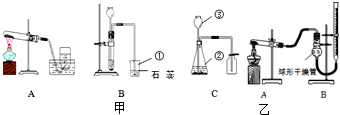
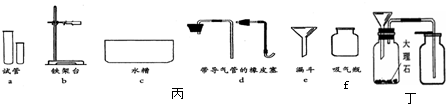
以氯酸钾与二氧化锰的混合物制氧气的装置和实验室制二氧化碳的装置,是初中化学中的二个典型的气体发生装置,它们还能够制取其它很多气体.
(1)硫化氢气体是一种易溶于水,密度大于空气的气体,实验室中常用固体硫化亚铁和浓硫酸反应来制得,硫化氢气体在空气中燃烧生成二氧化硫和水.根据上述信息,完成下列各题.
①实验室制硫化氢气体应用
(2)甲烷是一种极难溶于水的密度小于空气的气体,实验室中常用醋酸钠和碱石灰二种固体粉末混合加热来制取,则实验室制甲烷应用
(1)硫化氢气体是一种易溶于水,密度大于空气的气体,实验室中常用固体硫化亚铁和浓硫酸反应来制得,硫化氢气体在空气中燃烧生成二氧化硫和水.根据上述信息,完成下列各题.
①实验室制硫化氢气体应用
制二氧化碳
制二氧化碳
(氯酸钾制氧气或制二氧化碳)的装置;②硫化氢气体的收集方法是向上排空气法
向上排空气法
;③实验室制硫化氢气体的化学方程式是FeS+H2SO4═FeSO4+H2S↑
FeS+H2SO4═FeSO4+H2S↑
;④硫化氢气体燃烧的化学方程式为2H2S+3O2
2SO2+2H2O
| ||
2H2S+3O2
2SO2+2H2O
.
| ||
(2)甲烷是一种极难溶于水的密度小于空气的气体,实验室中常用醋酸钠和碱石灰二种固体粉末混合加热来制取,则实验室制甲烷应用
氯酸钾制氧气
氯酸钾制氧气
(氯酸钾制氧气或制二氧化碳)的装置.收集方法可用①向下排空气法
向下排空气法
;②排水法
排水法
.分析:(1)根据药品的状态和反应条件选择气体的制取装置,根据气体的密度和溶解性选择气体的收集方法,然后结合实验室中常用固体硫化亚铁和浓硫酸反应来制得,硫化氢气体是一种易溶于水,密度大于空气的气体,氯化亚铁和稀硫酸反应生成硫酸亚铁和硫化氢,硫化氢气体在空气中燃烧生成二氧化硫和水即可解答;
(2)根据实验室中常用醋酸钠和碱石灰二种固体粉末混合加热来制取选择发生装置和甲烷是一种极难溶于水的密度小于空气的气体选择收集方法解答.
(2)根据实验室中常用醋酸钠和碱石灰二种固体粉末混合加热来制取选择发生装置和甲烷是一种极难溶于水的密度小于空气的气体选择收集方法解答.
解答:解:(1)实验室中常用固体硫化亚铁和浓硫酸反应来制得,硫化氢气体是一种易溶于水,密度大于空气的气体,氯化亚铁和稀硫酸反应生成硫酸亚铁和硫化氢,硫化氢气体在空气中燃烧生成二氧化硫和水,
故答案:①制二氧化碳;②向上排空气法;③FeS+H2SO4═FeSO4+H2S↑;④2H2S+3O2
2SO2+2H2O.
(2)实验室中常用醋酸钠和碱石灰二种固体粉末混合加热所以选用氯酸钾制氧气,甲烷是一种极难溶于水的密度小于空气的气体,所以既可选用排水法也可选用向下排空气法,
故答案:氯酸钾制氧气;①向下排空气法②排水法.
故答案:①制二氧化碳;②向上排空气法;③FeS+H2SO4═FeSO4+H2S↑;④2H2S+3O2
| ||
(2)实验室中常用醋酸钠和碱石灰二种固体粉末混合加热所以选用氯酸钾制氧气,甲烷是一种极难溶于水的密度小于空气的气体,所以既可选用排水法也可选用向下排空气法,
故答案:氯酸钾制氧气;①向下排空气法②排水法.
点评:本题属于扩展性问题,重在考查根据物质的反应物和反应条件选取装置.

练习册系列答案
相关题目
某化学兴趣小组利用下列装置进行O2、CO2的实验室制法和有关性质的研究.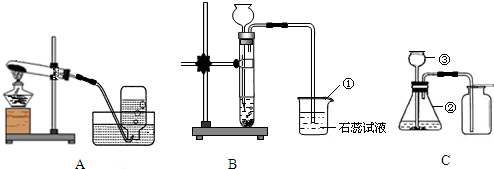
(1)写出下列编号仪器的名称:① ;② ③
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的 装置(填编号).用化学方程式表示反应原理 .当O2收集满,取出集气瓶后,停止该实验的正确操作步骤是先 ,后 .
(3)为了较准确测定KMnO4完全分解产生氧气的体积,可进行以下试验:称取9.5g KMnO4加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空:测量气体体积时,可以将反应发生装置和收集装置中的气体冷却至室温再进行.则收集气体应选下图中的装置 才合理(填编号),理由是 .
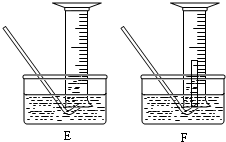
(4)乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释是 (填序号)
A、产生的CO2直接使石蕊试液变红
B、产生的CO2与水反应生成H2CO3使石蕊试液变红
C、挥发出的氯化氢溶于水使石蕊试液变红
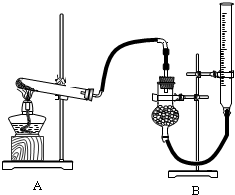
(5)实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解,现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,用下图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表
:
回答下列问题:
①上述实验中的“待测数据”指 ;
②本实验装置图中量气装置B由球形干燥管、乳胶管和50mL滴定管(带刻度)改造后组装而成,此处所用液体通常选 (填字母编号);
A、水;B、浓硫酸;C、双氧水;D、无水酒精
③若要证明实验②中球形干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞, ,观察现象;
④为探究CuO在实验
(6)中是否起催化作用,需补做如下实验(无需写出具体操作):
A、 B、CuO的化学性质有没有改变.

(1)写出下列编号仪器的名称:①
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的
(3)为了较准确测定KMnO4完全分解产生氧气的体积,可进行以下试验:称取9.5g KMnO4加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空:测量气体体积时,可以将反应发生装置和收集装置中的气体冷却至室温再进行.则收集气体应选下图中的装置

(4)乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释是
A、产生的CO2直接使石蕊试液变红
B、产生的CO2与水反应生成H2CO3使石蕊试液变红
C、挥发出的氯化氢溶于水使石蕊试液变红
(5)实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解,现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,用下图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表
:

| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其它物质 | |
| ⑤ | 1.2g | CuO0.5g | |
| ⑥ | 1.2g | MnO20.5g |
①上述实验中的“待测数据”指
②本实验装置图中量气装置B由球形干燥管、乳胶管和50mL滴定管(带刻度)改造后组装而成,此处所用液体通常选
A、水;B、浓硫酸;C、双氧水;D、无水酒精
③若要证明实验②中球形干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
④为探究CuO在实验
(6)中是否起催化作用,需补做如下实验(无需写出具体操作):
A、
 实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解,现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较(即比较反应的快慢).用如图装置进行实验,实验时均以生成25mL气体为准,其他可能影响实验的因素已忽略,相关数据见下表:
实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解,现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较(即比较反应的快慢).用如图装置进行实验,实验时均以生成25mL气体为准,其他可能影响实验的因素已忽略,相关数据见下表: