题目内容
 如图是某氮肥包装的部分内容.
如图是某氮肥包装的部分内容.(1)请你通过计算证明该包装中的广告宣传为虚假宣传(结果保留1位小数).
(2)红星村在春耕来临之际计划给农田施加氮肥补充氮元素,原计划购买300吨含尿素80%的氮肥(假设杂质中不含氮元素),后因种种原因改用硝酸铵(NH4NO3),要达到同样的补充氮元素的效果,则应用硝酸铵的质量是多少?
分析:(1)欲正确解答本题,需先计算出尿素中氮元素的质量分数,而后进行比较即可;
(2)先计算尿素中氮元素的质量,进而求的硝酸铵的质量.
(2)先计算尿素中氮元素的质量,进而求的硝酸铵的质量.
解答:解:(1)在CO(NH2)2中氮元素的质量分数=
×100%=46.7%<48%,因此该广告虚假;
(2)尿素中氮元素的质量300t×80%×
×100%=112t;
要达到同样的补充氮元素的效果,则应用硝酸铵的质量为112t÷
×100%=320t.
答:(1)在CO(NH2)2中氮元素的质量分数=
×100%=46.7%<48%,因此该广告虚假;
(2)要达到同样的补充氮元素的效果,则应用硝酸铵的质量为320t.
| 14x2 |
| 12+16+16x2 |
(2)尿素中氮元素的质量300t×80%×
| 28 |
| 60 |
要达到同样的补充氮元素的效果,则应用硝酸铵的质量为112t÷
| 28 |
| 80 |
答:(1)在CO(NH2)2中氮元素的质量分数=
| 14x2 |
| 12+16+16x2 |
(2)要达到同样的补充氮元素的效果,则应用硝酸铵的质量为320t.
点评:本题主要考查学生运用元素的质量分数公式进行计算的能力.

练习册系列答案
相关题目
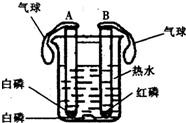 (1)如图为某学生设计的探究可燃物燃烧条件的实验,请回答:
(1)如图为某学生设计的探究可燃物燃烧条件的实验,请回答:①反应中观察到的现象是
②该实验设计的特点有
③待发生燃烧反应的试管冷却后,小明将试管倒立在水槽的水中,捏住气球口部,小心取下气球,观察试管中的现象是
(2)如图所示是一种氮肥的包装标签.请回答下列问题:(以下计算结果均保留至0.1%)
| 碳酸氢铵 NH4HCO3 净重:50kg 含氮量:16.8% ×××化学工业公司①碳酸氢铵中氮元素的质量分数是 ②这种氮肥的纯度(即化肥中碳酸氢铵的质量分数)是
(1)如图为某学生设计的探究可燃物燃烧条件的实验,请回答:
①反应中观察到的现象是______. ②该实验设计的特点有______. ③待发生燃烧反应的试管冷却后,小明将试管倒立在水槽的水中,捏住气球口部,小心取下气球,观察试管中的现象是______,产生此现象的原因是______. (2)如图所示是一种氮肥的包装标签.请回答下列问题:(以下计算结果均保留至0.1%)
②这种氮肥的纯度(即化肥中碳酸氢铵的质量分数)是______. 
(2008?塘沽区三模)(1)如图为某学生设计的探究可燃物燃烧条件的实验,请回答:
①反应中观察到的现象是______. ②该实验设计的特点有______. ③待发生燃烧反应的试管冷却后,小明将试管倒立在水槽的水中,捏住气球口部,小心取下气球,观察试管中的现象是______,产生此现象的原因是______. (2)如图所示是一种氮肥的包装标签.请回答下列问题:(以下计算结果均保留至0.1%)
②这种氮肥的纯度(即化肥中碳酸氢铵的质量分数)是______.  |
