题目内容
10.在由CH4和H2组成的混合气体中,碳元素的质量分数为60%,则混合气体充分燃烧后生成CO2和H2O的质量比是( )| A. | 11:18 | B. | 22:9 | C. | 11:37 | D. | 1:1 |
分析 依据混合气体中碳元素的质量分数求出碳氢元素质量比进行解答.
解答 解:气体中C、H元素质量比为:60%:40%=3:2
其中C、H原子个数比:$\frac{3}{12}$:$\frac{2}{1}$=1:8;所以二氧化碳和水的分子个数比为:$\frac{1}{1}$:$\frac{8}{2}$=1:4,二氧化碳和水的质量比为(1×44):(4×18)=11:18
故选A.
点评 本题考查学生根据物质中元素的质量百分数进行分析解题的能力.

练习册系列答案
相关题目
20.元素X的原子的第二层有6个电子,元素Y的原子的第三层有2个电子,则X和Y所形成化合物的化学式表示为( )
| A. | XY | B. | YX | C. | X2Y | D. | Y2X |
1.下列实验现象描述正确的是( )
| A. | 氢气在空气中燃烧时,产生淡蓝色火焰 | |
| B. | 细铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 用力振荡盛有水和植物油的试管,得到澄清透明的液体 | |
| D. | 把银片插入硫酸铜溶液中,一段时间后取出,银片表面有一层红色物质 |
5.下列物质的用途中,主要利用其化学性质的是( )
| A. | 氧气用于炼钢 | B. | 干冰用作制冷剂 | C. | 水银用于温度计 | D. | 石墨制铅笔芯 |
 化学是一门实验科学,观察或动手,会启迪你的智慧.以下几个实验是老师,或是你亲自做过的,请你按要求填写合理解释或现象.
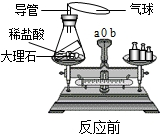
化学是一门实验科学,观察或动手,会启迪你的智慧.以下几个实验是老师,或是你亲自做过的,请你按要求填写合理解释或现象. 为测定某市售CaCO3药品中CaCO3的质量分数(杂质为SiO2,与稀HCl不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中CaCO3的质量,从而计算出样品中CaCO3的质量分数.为测定生成CO2的质量,他设计了如图的实验方案(已知;无水氯化钙是常见的干燥剂):
为测定某市售CaCO3药品中CaCO3的质量分数(杂质为SiO2,与稀HCl不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中CaCO3的质量,从而计算出样品中CaCO3的质量分数.为测定生成CO2的质量,他设计了如图的实验方案(已知;无水氯化钙是常见的干燥剂):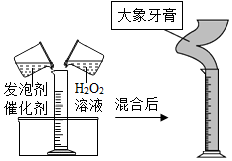 实验小组同学做了如图所示的实验.
实验小组同学做了如图所示的实验.