题目内容
为了测定空气中氧气的含量,某同学设计装置如图1,
(1)将红磷点燃后,伸入到集气瓶中,看到的现象①______;
反应冷却后,打开止水夹后看到的现象②______.【①、②描述关键现象即可得分】,此反应的化学方程式为:③______ 2P2O5
【答案】分析:(1)依据红磷燃烧的实验现象及测定装置的情况判断即可.
(2)题目要求分析可能造成测量结果小于 的原因,不仅仅是产生误差,而是强调小于
的原因,不仅仅是产生误差,而是强调小于 ,所以要围绕偏低的各种可能进行分析.
,所以要围绕偏低的各种可能进行分析.
(3)根据木炭燃烧生成物是气体二氧化碳分析压强的变化;
(4)根据空气中氧气含量约占 进行分析计算;
进行分析计算;
解答:解:(1)实验中观察到的现象是:红磷燃烧产生大量白烟,放出热量,打开弹簧夹后,有水进入集气瓶,水位上升约
化学方程式为:4P+5O2 2P2O5
2P2O5
(2)空气中氧气含量的测定,对实验的成败注意事项为:要保证药品过量,要保证装置的气密性良好,同时一定要等到温度恢复到室温再打开止水夹让外界液体进入装置内.所以在分析造成装置造成结果小于 时,要考虑药品的量可能不足造成没有将氧气完全消耗,同时要考虑装置在药品的足够的情况下因为气密性不好,导致液体不能等体积进入而引起结果偏低以及温度对实验结果的影响.
时,要考虑药品的量可能不足造成没有将氧气完全消耗,同时要考虑装置在药品的足够的情况下因为气密性不好,导致液体不能等体积进入而引起结果偏低以及温度对实验结果的影响.
(3)木炭燃烧产生CO2是气体,瓶内压强不变,水不会倒流,实验不会成功;
(4)氧气约占空气体积的 ,空气总体积为50mL,所以氧气约占10mL,氧气被消耗尽,剩余气体体积约为40mL;
,空气总体积为50mL,所以氧气约占10mL,氧气被消耗尽,剩余气体体积约为40mL;
故答案为:(1)红磷剧烈燃烧,产生大量白烟;烧杯中的水沿导管流入集气瓶中RH 约占剩余体积的五分之一;
4P+5O2 2P2O5
2P2O5
(2)红 磷的量不足或装置漏气或没等装置冷却就打开了弹簧夹;
(3)木炭燃烧产生CO2是气体,瓶内压强不变,水不会倒流
(4)40
点评:本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,属于常规性实验考查题.
(2)题目要求分析可能造成测量结果小于
 的原因,不仅仅是产生误差,而是强调小于
的原因,不仅仅是产生误差,而是强调小于 ,所以要围绕偏低的各种可能进行分析.
,所以要围绕偏低的各种可能进行分析.(3)根据木炭燃烧生成物是气体二氧化碳分析压强的变化;
(4)根据空气中氧气含量约占
 进行分析计算;
进行分析计算;解答:解:(1)实验中观察到的现象是:红磷燃烧产生大量白烟,放出热量,打开弹簧夹后,有水进入集气瓶,水位上升约

化学方程式为:4P+5O2
 2P2O5
2P2O5(2)空气中氧气含量的测定,对实验的成败注意事项为:要保证药品过量,要保证装置的气密性良好,同时一定要等到温度恢复到室温再打开止水夹让外界液体进入装置内.所以在分析造成装置造成结果小于
 时,要考虑药品的量可能不足造成没有将氧气完全消耗,同时要考虑装置在药品的足够的情况下因为气密性不好,导致液体不能等体积进入而引起结果偏低以及温度对实验结果的影响.
时,要考虑药品的量可能不足造成没有将氧气完全消耗,同时要考虑装置在药品的足够的情况下因为气密性不好,导致液体不能等体积进入而引起结果偏低以及温度对实验结果的影响.(3)木炭燃烧产生CO2是气体,瓶内压强不变,水不会倒流,实验不会成功;
(4)氧气约占空气体积的
 ,空气总体积为50mL,所以氧气约占10mL,氧气被消耗尽,剩余气体体积约为40mL;
,空气总体积为50mL,所以氧气约占10mL,氧气被消耗尽,剩余气体体积约为40mL;故答案为:(1)红磷剧烈燃烧,产生大量白烟;烧杯中的水沿导管流入集气瓶中RH 约占剩余体积的五分之一;
4P+5O2
 2P2O5
2P2O5(2)红 磷的量不足或装置漏气或没等装置冷却就打开了弹簧夹;
(3)木炭燃烧产生CO2是气体,瓶内压强不变,水不会倒流
(4)40
点评:本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,属于常规性实验考查题.

练习册系列答案
相关题目
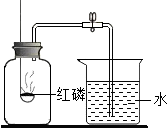 为了测定空气中氧气的体积分数,按右图装置进行实验:
为了测定空气中氧气的体积分数,按右图装置进行实验: 为了测定空气中氧气的含量,如图,(1)将红磷点燃后,伸到集气瓶中产生的现象是:
为了测定空气中氧气的含量,如图,(1)将红磷点燃后,伸到集气瓶中产生的现象是: 某兴趣小组同学按照如图实验装置进行实验,请回 答相关问题:
某兴趣小组同学按照如图实验装置进行实验,请回 答相关问题: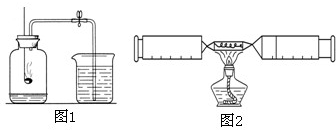
 注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动:
注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动: