题目内容
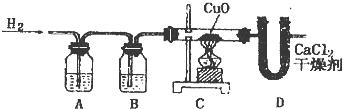
利用氢气还原灼热的氧化铜的实验测定水的组成(装置如图),得到下列结果。
氧化铜和玻璃管在通入氢气前的总质量是56g;在通入氢气完全反应后的总质量为51.2g;氯化钙和U形管在实验前的总质量是104.6g;在实验后的总质量是110g,求
(1)完全反应后生成水的质量。
(2)生成的水中氧的质量。
(3)生成的水中氢的质量。
(4)水中氢和氧的质量比。
答案:
解析:
提示:
解析:
| 解:氯化钙和U形管实验后总质量的增加,是因为吸收了氢气还原氧化铜生成的水。所以实验前后总质量之差即是生成水的质量。氧化铜失去氧还原成铜,质量减少,所以氧化铜和玻璃管在反应前后的总质量之差,即是氧化铜失去氧的质量。是氢气夺取了氧化铜的氧,并与之化合生成水,所以生成的水中氧的质量即是氧化铜失去氧的质量。水的质量减去水中氧的质量,就是水中氢元素的质量。
(1)生成水的质量:110g-104.6g=5.4g (2)生成水中氧的质量:56g-51.2g=4.8g (3)生成的水中氢的质量:5.4g-4.8g=0.6g (4)水中氢和氧的质量比:0.6g∶4.8g=1∶8
|
提示:

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目