题目内容
1.化学与生活密切相关①生活中常用稀盐酸来除铁锈,将一生锈的铁钉放入一杯稀盐酸中,不一会发现溶液变黄色,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O;接下来又发现有气泡产生,是因为铁和盐酸发生了反应,由此说明锈铁钉不能长时间浸泡在酸溶液中.
②我们通常测得正常雨水检验其pH<7,这是因为溶解有二氧化碳的原因.如果当雨水的PH<5.6,则称为酸雨.
③熟石灰的主要化学成分是Ca(OH)2(填化学式),它由生石灰与水反应得到,其反应的化学方程式是CaO+H2O═Ca(OH)2.用熟石灰制成的石灰浆刷墙壁,过几天就变得白而坚硬,其变化过程的化学方程式是Ca(OH)2+CO2═CaCO3↓+H2O.
分析 ①铁锈的主要成分是氧化铁,氧化铁能与盐酸反应生成氯化铁和水,氯化铁的水溶液呈黄色,铁锈除去后铁与盐酸反应生成氯化亚铁和氢气,据此解答;
②空气中含有二氧化碳,二氧化碳能和雨水反应生成碳酸,碳酸显酸性,所以正常的雨水常呈微酸性,如果当雨水的PH<5.6,则称为酸雨;
③熟石灰是氢氧化钙的俗称,可以由生石灰氧化钙与水反应生成,生成的氢氧化钙能与空气中的二氧化碳反应生成碳酸钙而变得坚硬.
解答 解:①铁锈的主要成分是氧化铁,氧化铁能与盐酸反应生成氯化铁和水,氯化铁的水溶液呈黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;铁锈除去后铁与盐酸反应生成氯化亚铁和氢气;
②空气中含有二氧化碳,二氧化碳能和雨水反应生成碳酸,碳酸显酸性,所以正常的雨水常呈微酸性,如果当雨水的PH<5.6,则称为酸雨;
③熟石灰的主要成分是氢氧化钙,可以由生石灰氧化钙与水反应生成,生成的氢氧化钙能与空气中的二氧化碳反应生成碳酸钙和水,化学方程式分别为:CaO+H2O═Ca(OH)2,Ca(OH)2+CO2═CaCO3↓+H2O;
故答案为:①Fe2O3+6HCl═2FeCl3+3H2O;铁,盐酸;
②二氧化碳;酸;
③Ca(OH)2;生石灰;CaO+H2O═Ca(OH)2,Ca(OH)2+CO2═CaCO3↓+H2O;
点评 完成此题,可以依据已有的知识进行,要求同学们在平时的学习中加强基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
12.研究和控制化学反应条件有重要意义.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响,在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
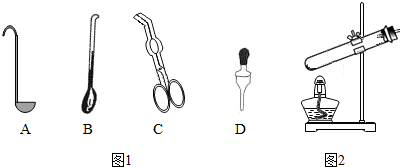
①取用二氧化锰的仪器是图1中的B(选填编号).
②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响,在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
16.以下不能与水混合产生溶液的是( )
| A. | 可乐 | B. | 稀盐酸 | C. | 食用油 | D. | 蔗糖 |
6.某化学兴趣小组对一包干燥的红色粉末组成进行探究.请你参与并回答问题:
【教师提醒】它由Cu、Fe2O3两种固体中的一种或两种组成
【提出猜想】红色粉末可能的组成:
猜想①只有Cu; 猜想②只有Fe2O3; 猜想③是Cu、Fe2O3的混合物
【实验探究】
同学们为确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,如图1在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,继续通CO气体直至玻璃管冷却.
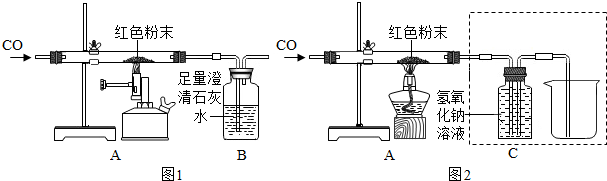
(1)在装置A中先通CO气体的目的是排净装置中的空气,防止加热时发生爆炸,A装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)反应前后称量相关装置和物质的总质量,其数据如下表:
小丁同学分析表中的数据后,得出的结论是猜想③成立.
(3)小林同学认为为了防止溶液倒吸,本实验停止加热前应先断开A和B的连接,小丽认为不需要,理由是因为一直通入CO气体,B中溶液不会倒吸到A装置中.
【反思评价】实验后小组内有同学指出:上图装置未进行尾气的处理.于是有同学设计了用图2装置代替原装置,实验装置图中采用虚线框内的装置,其作用有AB.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
【教师提醒】它由Cu、Fe2O3两种固体中的一种或两种组成
【提出猜想】红色粉末可能的组成:
猜想①只有Cu; 猜想②只有Fe2O3; 猜想③是Cu、Fe2O3的混合物
【实验探究】
同学们为确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,如图1在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,继续通CO气体直至玻璃管冷却.

(1)在装置A中先通CO气体的目的是排净装置中的空气,防止加热时发生爆炸,A装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)反应前后称量相关装置和物质的总质量,其数据如下表:
| 反应前 | 反应后 |
| 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
(3)小林同学认为为了防止溶液倒吸,本实验停止加热前应先断开A和B的连接,小丽认为不需要,理由是因为一直通入CO气体,B中溶液不会倒吸到A装置中.
【反思评价】实验后小组内有同学指出:上图装置未进行尾气的处理.于是有同学设计了用图2装置代替原装置,实验装置图中采用虚线框内的装置,其作用有AB.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
13.下列有关实验现象的描述正确的是( )
| A. | 铁丝在氧气中燃烧生成黑色固体 | B. | 镁条在空气中燃烧产生白色烟雾 | ||
| C. | 氢气在空气中燃烧产生黄色火焰 | D. | 硫在氧气中燃烧产生淡蓝色的火焰 |

 金属材料与人类的生产和生活密切相关.请回答:
金属材料与人类的生产和生活密切相关.请回答: