题目内容
16.在CO和CO2的混合气体中,含碳元素36%,将该混合气体5g通过足量灼热的氧化铜,完全反应后,气体再通入足量的澄清石灰水中,得到的白色沉淀质量是( )| A. | 5g | B. | 10g | C. | 15g | D. | 20g |
分析 因为混合气体通过足量的氧化铜后,气体就都变成了二氧化碳;那么,5g混合气体中含的碳,最后都变成二氧化碳,由题意中“通入足量的澄清石灰水”然后都变成碳酸钙,利用碳元素的守恒就可以计算了.
解答 解:5.0g该气体混合物中碳的质量=5g×36%=1.8g;所以 CaCO3中碳的质量为1.8g,
又因为碳酸钙中碳元素的质量分数=$\frac{碳原子的相对原子质量}{碳酸钙的相对分子质量}$×100%=$\frac{12}{100}$×100%=12%,
所以白色沉淀碳酸钙的质量=$\frac{1.8g}{12%}$=15g
答案:C.
点评 本题考查了根据化学方程式中元素的质量守恒来计算所求的生成的物质,方法多种;但是根据某元素的质量守恒更简单,培养学生的实际解决问题能力.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
6.下列成语包含化学变化的是( )
| A. | 刻舟求剑 | B. | 火树银花 | C. | 风吹草动 | D. | 量体裁衣 |
11.下列实验操作正确的是( )
| A. |  | B. |  | ||
| C. | 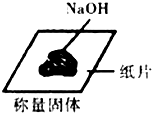 | D. | 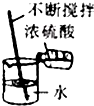 |


 小明看到家里××牌钙片的说明书,部分文字说明如图所示,他对该钙片的含钙量有疑问,于是取出10片做探究实验.当加入50g溶质质量分数为7.3%的稀盐酸时,二者恰好完全反应.
小明看到家里××牌钙片的说明书,部分文字说明如图所示,他对该钙片的含钙量有疑问,于是取出10片做探究实验.当加入50g溶质质量分数为7.3%的稀盐酸时,二者恰好完全反应.