题目内容
 某同学做了一个如下实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球悬浮于液面,位置如图所示.将从废电池外壳收集来的锌粒放入烧杯中,该学生看到的现象是
某同学做了一个如下实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球悬浮于液面,位置如图所示.将从废电池外壳收集来的锌粒放入烧杯中,该学生看到的现象是考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据锌片与盐酸反应后溶液的溶质的相对分子质量的改变,推出溶液密度的变化,即溶质相对分子质量越大,溶液密度越大,溶质相对分子质量越小,溶液密度越小; 漂浮满足的条件为重力等于浮力,由于重力不变,则浮力不变,则应该是排开液体的体积减少,因此应该上浮
解答:解:
锌的金属活动性在H前,因此可与酸反应生成H2;当锌与稀盐酸反应后,溶液中的溶质发生了改变,由HCl变成了ZnCl2,其相对分子质量增大了,根据ρ=m/v,在体积没有明显改变的情况下,溶液密度ρ也相应增大;而根据浮力F=ρvg和漂浮满足的条件为重力等于浮力,由于重力不变,则浮力不变.则应该是排开液体的体积减少,因此应该上浮.
故答案为:产生气泡,锌片逐渐溶解,小球移动、上浮;上浮;因为锌与盐酸反应生成了氯化锌,溶质的相对分子质量增大,使得溶液的密度增大,而漂浮满足的条件为重力等于浮力,由于重力不变,则浮力不变,则应该是排开液体的体积减少,因此应该上浮;Zn+2HCl═ZnCl2+H2↑
锌的金属活动性在H前,因此可与酸反应生成H2;当锌与稀盐酸反应后,溶液中的溶质发生了改变,由HCl变成了ZnCl2,其相对分子质量增大了,根据ρ=m/v,在体积没有明显改变的情况下,溶液密度ρ也相应增大;而根据浮力F=ρvg和漂浮满足的条件为重力等于浮力,由于重力不变,则浮力不变.则应该是排开液体的体积减少,因此应该上浮.
故答案为:产生气泡,锌片逐渐溶解,小球移动、上浮;上浮;因为锌与盐酸反应生成了氯化锌,溶质的相对分子质量增大,使得溶液的密度增大,而漂浮满足的条件为重力等于浮力,由于重力不变,则浮力不变,则应该是排开液体的体积减少,因此应该上浮;Zn+2HCl═ZnCl2+H2↑
点评:同学们要学会判断化学反应后溶液中溶质的判断,并根据其相对分子质量的变化判断出溶液密度的变化.

练习册系列答案
相关题目
在下列物质的变化中,不能用质量守恒定律解释的是( )
| A、煤燃烧后剩余煤渣的质量小于煤的质量 |
| B、铁丝燃烧后质量增大 |
| C、铁生锈以后总质量比原来铁的质量大 |
| D、水结成冰以后,冰的质量与水的质量相等 |
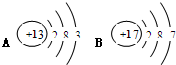 “用微观的眼光看世界”是学习化学的重要方法,按要求填空.
“用微观的眼光看世界”是学习化学的重要方法,按要求填空.