题目内容
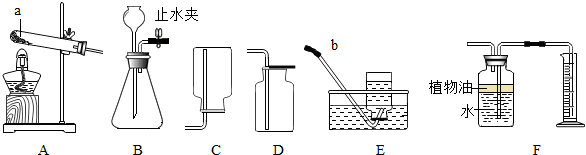
 在学习“铁的冶炼”后,兴趣小组的同学按课本装置图进行改装实验(如图所示),反应后玻璃管中红色粉末变成了黑色粉末A,请你用化学方程式表示该炼铁原理:
在学习“铁的冶炼”后,兴趣小组的同学按课本装置图进行改装实验(如图所示),反应后玻璃管中红色粉末变成了黑色粉末A,请你用化学方程式表示该炼铁原理:【提出问题】黑色粉末A是不是全部是铁?
【查阅资料】铁的氧化物有Fe3O4、Fe2O3、FeO(氧化亚铁,黑色固体),都能与稀盐酸反应,且只有Fe3O4能被磁铁吸引.
【进行猜想】
(1)小明认为黑色粉末A全部是Fe.
(2)小华提出来猜想①和猜想②,请你补充猜想③.
猜想①:黑色粉末A由Fe和Fe3O4组成;
猜想②:黑色粉末A由Fe和FeO组成;
猜想③:黑色粉末A由Fe和
【实验探究】
(1)小明取适量黑色粉末A加入足量
(2)小华按下列方案继续探究,请你一同参与.
| 方案 | 实验操作及可能的现象 | 结论 |
| ① | 取适量黑色粉末A用磁铁吸引,黑色粉末全部被吸引 | 猜想①正确 |
| ② | 取适量黑色粉末B加入足量稀盐酸,黑色粉末全部溶解 | 猜想②正确 |
| ③ | 取适量 | 猜想③正确 |
【得出结论】通过上述实验得出黑色粉末A的成分.
【拓展延伸】铁锈的主要成分是Fe2O3?xH2O,人们常用
考点:实验探究物质的组成成分以及含量,金属的化学性质,一氧化碳还原氧化铁,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:根据炼铁的原理写出反应的化学方程式;根据一氧化碳有毒能污染空气分析装置的不足;
【进行猜想】根据铁的氧化物的颜色和性质进行猜想;
【实验探究】(1)根据铁能与硫酸铜反应分析判断;
(2)根据氧化亚铁不能被磁铁吸引,铁和四氧化三铁能被磁铁吸引、铁能与硫酸铜反应、四氧化三铁不能与硫酸铜分析验证猜想三.
【反思评价】根据四氧化三铁是黑色的能与盐酸反应分析方案②的结论;
【拓展延伸】根据铁锈能与盐酸反应分析除铁锈的方法.
【进行猜想】根据铁的氧化物的颜色和性质进行猜想;
【实验探究】(1)根据铁能与硫酸铜反应分析判断;
(2)根据氧化亚铁不能被磁铁吸引,铁和四氧化三铁能被磁铁吸引、铁能与硫酸铜反应、四氧化三铁不能与硫酸铜分析验证猜想三.
【反思评价】根据四氧化三铁是黑色的能与盐酸反应分析方案②的结论;
【拓展延伸】根据铁锈能与盐酸反应分析除铁锈的方法.
解答:解:在高温条件下,一氧化碳能将氧化铁还原出来生成了铁和二氧化碳,反应的方程式是:3CO+Fe2O3
2Fe+3CO2;一氧化碳有毒,能污染空气,应将尾气处理,从环保的角度考虑,该装置明显的不足是:缺少尾气处理装置;
【进行猜想】由于铁的氧化物Fe3O4、FeO、还原出的铁都是黑色的,所以猜想三是:黑色粉末A由Fe和氧化亚铁和四氧化三铁组成.
【实验探究】
(1)若黑色粉末A若只有铁粉,加入足量硫酸铜溶液后会全部发生反应,不会有黑色固体剩余,而实验过程中有黑色固体剩余,据此可知小明的猜想是错误的.
(2)由于氧化亚铁不能被磁铁吸引,铁、四氧化三铁能被磁铁吸引,铁能与硫酸铜反应、四氧化三铁不能与硫酸铜反应.所以实验③的设计方案及可能的现象是:
【反思评价】由于四氧化三铁是黑的,也能与盐酸反应,所以,方案②的结论不正确;
【拓展延伸】由于铁锈能与盐酸反应,所以,人们常用稀盐酸来清洗铁锈.
故答为:3CO+Fe2O3
2Fe+3CO2,缺少尾气处理装置;【进行猜想】黑色粉末A由Fe和氧化亚铁和四氧化三铁组成.【实验探究】(1)硫酸铜;(2)见上表;【反思评价】四氧化三铁能与盐酸反应;
【拓展延伸】稀盐酸.
| ||
【进行猜想】由于铁的氧化物Fe3O4、FeO、还原出的铁都是黑色的,所以猜想三是:黑色粉末A由Fe和氧化亚铁和四氧化三铁组成.
【实验探究】
(1)若黑色粉末A若只有铁粉,加入足量硫酸铜溶液后会全部发生反应,不会有黑色固体剩余,而实验过程中有黑色固体剩余,据此可知小明的猜想是错误的.
(2)由于氧化亚铁不能被磁铁吸引,铁、四氧化三铁能被磁铁吸引,铁能与硫酸铜反应、四氧化三铁不能与硫酸铜反应.所以实验③的设计方案及可能的现象是:
| 方案 | 实验操作及可能的现象 | 结论 |
| ③ | 取适量黑色粉末用磁铁吸引,黑色粉末未全部被吸引;取适上述被吸引的黑色粉末于试管中,加入足量硫酸铜溶液,仍有黑色固体剩余 | 猜想③正确 |
【拓展延伸】由于铁锈能与盐酸反应,所以,人们常用稀盐酸来清洗铁锈.
故答为:3CO+Fe2O3
| ||
【拓展延伸】稀盐酸.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.

练习册系列答案
相关题目
下列物质的用途与性质不对应的是( )
| A、食品包装中充氮气以防腐--常温下氮气的化学性质不活泼 |
| B、稀有气体能制成多种用途的电光源--稀有气体在通电时发出不同颜色的光 |
| C、一氧化碳用于冶炼金属--一氧化碳具有可燃性 |
| D、干冰可用做制冷剂--干冰升华吸热 |
下列实验操作错误的是( )
| A、过滤时用玻璃棒引流 |
| B、垫上石棉网加热盛液体的烧杯 |
| C、用手直接取用块状药品 |
| D、直接加热盛液体的蒸发皿 |
下列鉴别方法错误的是( )
| A、用水鉴别硝酸铵和氢氧化钠 |
| B、用燃烧的方法鉴别羊毛和合成纤维 |
| C、用燃烧的木条鉴别二氧化碳和氮气 |
| D、用紫色石蕊试液鉴别稀硫酸和蒸馏水 |
材料与人类生活密切相关.以下属于天然材料的是( )
| A、棉花 | B、塑料 | C、尼龙 | D、腈纶 |
 如图所示A、B、C、D、E都是九年级化学中常见的物质,且相邻物质间均能发生化学反应,A为常见的钾盐,A与B反应有气体生成,B与E反应有白色沉淀生成,C与E为同类物质,B、D均能用于除铁锈.
如图所示A、B、C、D、E都是九年级化学中常见的物质,且相邻物质间均能发生化学反应,A为常见的钾盐,A与B反应有气体生成,B与E反应有白色沉淀生成,C与E为同类物质,B、D均能用于除铁锈. 将CaCl2和NaCl的混合物20g放入90g水中使其完全溶解后,往其中加入Na2CO3溶液,加入Na2CO3溶液的质量与生成的沉淀质量的关系如图所示.
将CaCl2和NaCl的混合物20g放入90g水中使其完全溶解后,往其中加入Na2CO3溶液,加入Na2CO3溶液的质量与生成的沉淀质量的关系如图所示.