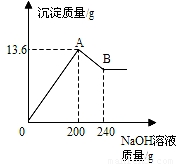
题目内容
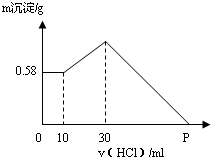 把NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中后,有0.58g白色沉淀.在所得浊液中逐滴加入18.25g/L的稀盐酸,加入盐酸体积与生成沉淀的质量关系如图所示.试求:
把NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中后,有0.58g白色沉淀.在所得浊液中逐滴加入18.25g/L的稀盐酸,加入盐酸体积与生成沉淀的质量关系如图所示.试求:(1)混合物中NaOH质量是多少克?
(2)混合物中AlCl3质量是多少克?
(3)P点所表示的盐酸体积是多少毫升?
分析:(1)由生成沉淀的质量关系图可知,滴加的前10mL稀盐酸,没有影响沉淀的量,说明滴加的稀盐酸在与混合物中剩余的氢氧化钠发生反应;继续滴加稀盐酸时,沉淀量增加,此时稀盐酸与NaAlO2发生反应产生Al(OH)3沉淀;此后再滴加的稀盐酸与氢氧化铝和氢氧化镁的沉淀发生反应,直至Mg(OH)2和Al(OH)3沉淀全部溶解;
综合以上分析,混合物中的氢氧化钠溶于水后与氯化镁、氯化铝发生反应后还有剩余,剩余的氢氧化钠与稀盐酸发生反应;
(2)根据以上的分析,固体物中的氯化铝与氢氧化钠反应生成NaAlO2;因此,计算出的质量就可以根据反应的化学方程式计算氯化铝的质量;
(3)P点为全部反应完全反应后所消耗稀盐酸的量,需要计算出氢氧化铝、氢氧化镁两种沉淀物完全溶解所消耗稀盐酸的量.
综合以上分析,混合物中的氢氧化钠溶于水后与氯化镁、氯化铝发生反应后还有剩余,剩余的氢氧化钠与稀盐酸发生反应;
(2)根据以上的分析,固体物中的氯化铝与氢氧化钠反应生成NaAlO2;因此,计算出的质量就可以根据反应的化学方程式计算氯化铝的质量;
(3)P点为全部反应完全反应后所消耗稀盐酸的量,需要计算出氢氧化铝、氢氧化镁两种沉淀物完全溶解所消耗稀盐酸的量.
解答:解:(1)由生成沉淀的质量关系图可知,混合物中有氢氧化钠剩余,则0.58g白色沉淀为混合物中氯化镁与氢氧化钠完全反应所生成的氢氧化镁;
设与氯化镁完全反应时消耗氢氧化钠的质量为x
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
80 58
x 0.58g
=
x=0.8g
设滴加10mL18.25g/L的稀盐酸消耗氢氧化钠的质量为y
NaOH+HCl═NaCl+H2O
40 36.5
y 10mL×10-3×18.25g/L
=
y=0.2g
与NaAlO2发生反应的盐酸的质量=(30-10)mL×10-3×18.25g/L=0.365g
设消耗20mL稀盐酸需要NaAlO2的质量为z
NaAlO2+HCl+H2O═Al(OH)3↓+NaCl
82 36.5
z 0.365g
=
z=0.82g
设生成0.82g需要消耗氢氧化钠的质量为a,同时需要AlCl3的质量为b
AlCl3+4NaOH═NaAlO2+3NaCl+2H2↑
3.5 160 82
b a 0.82g
=
a=1.6g
所以,混合物中NaOH质量=0.8g+0.2g+1.6g=2.6g
(2)
=
b=1.335g,即混合物中AlCl3质量是1.335g;
(3)由图知:P点溶液的溶质为NaCl、AlCl3、MgCl2,相当于用盐酸中和了原溶液中的NaOH所得的结果,
所以,设2.6g氢氧化钠完全反应需要稀盐酸的体积为v
NaOH+HCl═NaCl+H2O
40 36.5
2.6g v××10-3×18.25g/L
=
v=130mL
答:(1)混合物中NaOH质量是2.6g;
(2)混合物中AlCl3质量是1.335g;
(3)P点所表示的盐酸体积是130mL.
设与氯化镁完全反应时消耗氢氧化钠的质量为x
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
80 58
x 0.58g
| 80 |
| x |
| 58 |
| 0.58g |
x=0.8g
设滴加10mL18.25g/L的稀盐酸消耗氢氧化钠的质量为y
NaOH+HCl═NaCl+H2O
40 36.5
y 10mL×10-3×18.25g/L
| 40 |
| y |
| 36.5 |
| 10mL×10-3×18.25g/L |
y=0.2g
与NaAlO2发生反应的盐酸的质量=(30-10)mL×10-3×18.25g/L=0.365g
设消耗20mL稀盐酸需要NaAlO2的质量为z
NaAlO2+HCl+H2O═Al(OH)3↓+NaCl
82 36.5
z 0.365g
| 82 |
| z |
| 36.5 |
| 0.365g |
设生成0.82g需要消耗氢氧化钠的质量为a,同时需要AlCl3的质量为b
AlCl3+4NaOH═NaAlO2+3NaCl+2H2↑
3.5 160 82
b a 0.82g
| 160 |
| a |
| 82 |
| 0.82g |
a=1.6g
所以,混合物中NaOH质量=0.8g+0.2g+1.6g=2.6g
(2)
| 133.5 |
| b |
| 82 |
| 0.82g |
b=1.335g,即混合物中AlCl3质量是1.335g;
(3)由图知:P点溶液的溶质为NaCl、AlCl3、MgCl2,相当于用盐酸中和了原溶液中的NaOH所得的结果,
所以,设2.6g氢氧化钠完全反应需要稀盐酸的体积为v
NaOH+HCl═NaCl+H2O
40 36.5
2.6g v××10-3×18.25g/L
| 40 |
| 2.6g |
| 36.5 |
| v×10-3 ×18.25g/L |
v=130mL
答:(1)混合物中NaOH质量是2.6g;
(2)混合物中AlCl3质量是1.335g;
(3)P点所表示的盐酸体积是130mL.
点评:根据滴加稀盐酸与产生沉淀的关系图,分析各阶段所发生的反应,利用各阶段反应的化学方程式进行相关物质质量的计算;本题所涉及的反应比较复杂,在分析时逐个反应梳理清楚是解决本问题的关键.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
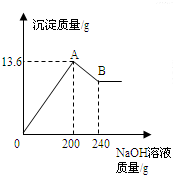 把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如图所示,试回答:(提示:Al(OH)3+NaOH═NaAlO2+2H2O,NaAlO2可溶于水)
把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如图所示,试回答:(提示:Al(OH)3+NaOH═NaAlO2+2H2O,NaAlO2可溶于水)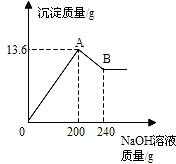 把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如下图所示.已知:NaOH与AlCl3反应时,先使AlCl3全部转化为不溶于水的Al(OH)3,然后Al(OH)3还能继续与过量的NaOH发生如下反应:Al(OH)3+NaOH═NaAlO2+2H2O,其中NaAlO2 是可溶于水的物质,试回答:
把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如下图所示.已知:NaOH与AlCl3反应时,先使AlCl3全部转化为不溶于水的Al(OH)3,然后Al(OH)3还能继续与过量的NaOH发生如下反应:Al(OH)3+NaOH═NaAlO2+2H2O,其中NaAlO2 是可溶于水的物质,试回答: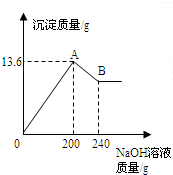 把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如图所示,试回答:(提示:Al(OH)3+NaOH═NaAlO2+2H2O,NaAlO2可溶于水)
把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如图所示,试回答:(提示:Al(OH)3+NaOH═NaAlO2+2H2O,NaAlO2可溶于水)