题目内容
19.一定质量的CaCO3与50克稀HCl恰好完全反应,生成CO22.2克试计算:(1)参加反应的CaCO3质量?
(2)所用稀HCl的质量分数?
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据二氧化碳质量可以计算碳酸钙质量和氯化氢的质量,进一步可以计算稀盐酸的质量分数.
解答 解:(1)设参加反应的CaCO3质量为x,反应的氯化氢质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 2.2g
$\frac{100}{x}$=$\frac{73}{y}$=$\frac{44}{2.2g}$,
x=5g,y=3.65g,
答:反应的碳酸钙质量是5g.
(2)所用稀HCl的质量分数为:$\frac{3.65g}{50g}$×100%=7.3%,
答:所用稀HCl的质量分数为7.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
9.下列物质间不能发生复分解反应的是( )
| A. | 碳酸钠溶液和氯化钙溶液 | B. | 氢氧化钾溶液与盐酸 | ||
| C. | 氢氧化钠溶液与氯化钾溶液 | D. | 硫酸铜溶液与氯化钡溶液 |
7.铁在氧气中燃烧的现象错误的是( )
| A. | 剧烈燃烧 | B. | 火星四射 | C. | 生成黑色固体 | D. | 生成四氧化三铁 |
14.下列物质中,由原子构成的是( )
| A. | 水银 | B. | 水 | C. | 液氧 | D. | 氯化钠 |
8.化学与生活息息相关.下列说法中不合理的是( )
| A. | 洗涤剂清洗油污是利用了洗涤剂的乳化作用 | |
| B. | 进入干涸的深井或菜窖前做灯火实验 | |
| C. | 室内用煤炉取暖,为防止热量散失,应关闭门窗 | |
| D. | 电器短路着火,应用干粉灭火器扑灭 |
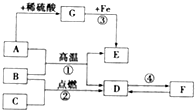 如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G是蓝色溶液,请根据如图回答下列问题:
如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G是蓝色溶液,请根据如图回答下列问题: 如图是电解水的示意图.
如图是电解水的示意图.