题目内容
1.现有10g铜粉与木炭粉的混合物,在空气中加热至质量不再发生变化,冷却后称量剩余固体的质量仍为1Og,则原混合物中铜粉与木炭粉的质量比为( )| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
分析 在空气中充分灼烧后会燃烧生成二氧化碳气体(碳粉完全消失),铜粉在空气中充分灼烧会生成氧化铜(铜粉质量增加).所以完全灼烧后的固体成分只有氧化铜.根据题意,完全灼烧后得到固体质量与原混合物相同,所以原混合物中炭粉与铜粉的质量比就等于参加反应氧气与铜粉的质量比.
解答 解:碳和铜都被完全氧化后,冷却到室温,发现固体的质量没有变化,说明碳的质量等于和铜反应的氧气的质量;
设铜的质量为x,参加反应的氧气的质量为y;
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO
128 32
x y
$\frac{x}{y}=\frac{128}{32}$=$\frac{4}{1}$
所以原混合物中铜粉与木炭粉的质量比为4:1
答案:D
点评 本题主要考查学生利用化学方程式进行计算的能力.本题的条件比较隐蔽,解题时需根据化学方程式认真分析数量关系,才能正确解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列实验基本操作正确的是( )
| A. |  点燃酒精灯 | B. |  液体的倾倒 | C. |  过滤 | D. |  稀释浓硫酸 |
12.下列实验操作正确的是( )
| A. |  铁丝在氧气中燃烧 | B. |  检查气密性 | ||
| C. |  稀释浓硫酸 | D. |  称量氢氧化钠固体 |
9.下列金属活动性最强的是( )
| A. | 银 | B. | 铁 | C. | 铜 | D. | 锌 |
16.以下对气体发生装置的选择或改进合理的是( )


| A. | 用装置①制备CO2可随时发生或停止反应 | |
| B. | 装置②可作实验室制备氧气 | |
| C. | 装置③可作实验室制备氢气 | |
| D. | 用装置④制取氧气可控制反应速率 |
6.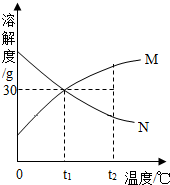 如图是M、N两种物质的溶解度曲线.t1℃时,往盛有100g水的烧杯中先后加入50gM和50gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.此时溶液的温度为t1℃,下列说法错误的是( )
如图是M、N两种物质的溶解度曲线.t1℃时,往盛有100g水的烧杯中先后加入50gM和50gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.此时溶液的温度为t1℃,下列说法错误的是( )
 如图是M、N两种物质的溶解度曲线.t1℃时,往盛有100g水的烧杯中先后加入50gM和50gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.此时溶液的温度为t1℃,下列说法错误的是( )
如图是M、N两种物质的溶解度曲线.t1℃时,往盛有100g水的烧杯中先后加入50gM和50gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.此时溶液的温度为t1℃,下列说法错误的是( )| A. | t1℃时,得到M、N的溶液是饱和溶液 | |
| B. | 将溶液的温度升为t2℃时,M、N物质溶液溶质的质量分数相等 | |
| C. | 温度降低时,N物质溶质的质量分数增大 | |
| D. | 温度为t1℃时,恒温蒸发10g水,结晶析出的M、N质量相等 |
13.安福火腿,名扬世界,火腿中的瘦肉富含的营养素为( )
| A. | 蛋白质 | B. | 维生素 | C. | 糖类 | D. | 油脂 |
 (1)盐酸、硫酸是常见的两种酸.①打开装浓盐酸的试剂瓶时,瓶口出现白雾,说明浓盐酸具有挥发性.②用水稀释浓硫酸时,将浓硫酸沿烧杯壁缓慢的注入盛有水的烧杯里并用玻璃棒不断搅拌即可.
(1)盐酸、硫酸是常见的两种酸.①打开装浓盐酸的试剂瓶时,瓶口出现白雾,说明浓盐酸具有挥发性.②用水稀释浓硫酸时,将浓硫酸沿烧杯壁缓慢的注入盛有水的烧杯里并用玻璃棒不断搅拌即可.