题目内容
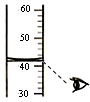
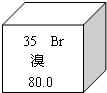 溴在制药、感光材料方面有着独特的作用.如图是溴元素在元素周期表中的截图.下列有关叙述不正确的是
溴在制药、感光材料方面有着独特的作用.如图是溴元素在元素周期表中的截图.下列有关叙述不正确的是
- A.溴属于非金属元素
- B.溴单质常温下为液态
- C.溴原子的中子数为35
- D.溴的相对原子质量为80.0
C
分析:根据元素周期表中的一个小格所提供的信息,原子序数=核外电子数=质子数=35,相对原子质量80.0,及元素符号、名称,进行判断.
解答:A、非金属元素名称一般有“氵”、“气”、“石”字旁,故A正确;
B、液态非金属元素名称有“氵”字旁,故B正确;
C、溴原子的质子数数为35,中子数为80-35=45,故C错误;
D、根据元素周期表中提供的信息可知:溴元素的相对原子质量是80.0,故D正确;
故选C.
点评:本题考查了元素周期表中看图回答最简单的元素名称、符号、原子序数、相对原子质量,学生必须掌握的知识.
分析:根据元素周期表中的一个小格所提供的信息,原子序数=核外电子数=质子数=35,相对原子质量80.0,及元素符号、名称,进行判断.
解答:A、非金属元素名称一般有“氵”、“气”、“石”字旁,故A正确;
B、液态非金属元素名称有“氵”字旁,故B正确;
C、溴原子的质子数数为35,中子数为80-35=45,故C错误;
D、根据元素周期表中提供的信息可知:溴元素的相对原子质量是80.0,故D正确;
故选C.
点评:本题考查了元素周期表中看图回答最简单的元素名称、符号、原子序数、相对原子质量,学生必须掌握的知识.

练习册系列答案
相关题目
生活处处有化学,厨房中就蕴含着丰富的化学知识..
(1)下列厨房用品中属于有机合成高分子材料的是________.(填字母)

(2)下表是每100g小麦、大米中主要营养物质的含量.
| 蛋白质(g) | 糖类(g) | 油脂(g) | 维生素A(μg) | 维生素C(mg) | 钙 (mg) | 铁 (mg) | 锌 (mg) | |
| 小麦 | 9.4 | 75 | 1.4 | 11 | 0 | 25 | 0.6 | 0.2 |
| 大米 | 7.7 | 76.8 | 0.6 | 0 | 8 | 11 | 1.1 | 1.45 |
②中国人的饮食以小麦和大米为主,根据上表可看出,这两种食物中糖的含量都非常高,其中所含淀粉的化学式为(
C6H10O5)n,其相对分子质量是________.
(3)馒头、面包等发面食品的一个特点是面团中有许多小孔,它们使发面食品松软可口.通常在做这些食品的时候会加入发酵粉,发酵粉的主要成分是________和有机酸,根据以上信息说明发酵粉的作用可能是________(写出一条).
学习化学是为了应用化学,造福人类.
I.化学知识将在2008年北京奥运会的多个方面发挥重要的作用.
(1)举重运动员在抓杠铃前常擦一种白色粉末碳酸镁(MgCO3),则碳酸镁属于________(填序号);
A.酸 B.碱 C.盐 D.氧化物
(2)今年5月11日,奥运圣火来到福建,据悉奥运火炬的燃料为丙烷.请根据下表信息写出丙烷的化学式:;
| 物质 | 甲烷 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 化学式 | CH4 | C2H6 | ________ | C4 H10 | C5 H12 |
A.导热、导电性
B.耐腐蚀、硬度较大、密度小
C.有金属光泽、良好的延展性
Ⅱ.汶川大地震是新中国成立以来破坏性最强的一次地震.灾后防疫部门用2%的漂白粉溶液对环境进行喷洒杀菌消毒.现代工业采用把氯气和消石灰或石灰乳反应的方法制取漂白粉.
(1)已知反应的化学方程式为2Cl2+2Ca(OH)2═X+Ca(C10)2+2H2O,则X的化学式为________;
(2)商品漂白粉中含有Ca(ClO)2、Ca(OH)2、CaCl2等物质,其中有效成分是Ca(C1O)2,因此商品漂白粉是________(填“混合物”或“纯净物”);
(3)在化学反应中,物质所含元素的化合价发生变化的就是氧化还原反应.根据(1)化学方程式中的Cl元素化合价变化情况判断该反应________ (填“是”或“不是”)氧化还原反应;
(4)汶川大地震使当地居民的饮用水受污染,以下关于饮用水处理方法不合理的是(填序号).
A.用明矾使悬浮物沉降下来
B.用漂白粉进行消毒杀菌
C.只要无色透明的水就可以放心饮用
D.饮用前加热煮沸.