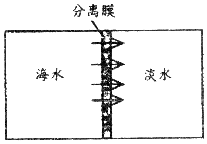
��Ŀ����
18��ijѧУ��ѧϰС��Ե��ص�ʯ��ʯ�������е��飬�ⶨʯ��ʯ��̼��Ƶ��������������õķ������£�ȡ��ʯ��ʯ��Ʒ20g����100gϡ������Ĵμ��룬���������������ݼ��±�����֪ʯ��ʯ��Ʒ�к��еĶ�����������ʲ�����ˮ��Ҳ����ϡ���ᷴӦ��������㣺| ��� | ����ϡ���������/g | ʣ����������/g |
| ��һ�� | 25 | 14 |
| �ڶ��� | 25 | 8 |
| ������ | 25 | 2.8 |
| ���Ĵ� | 25 | n |
��2��ʯ��ʯ��Ʒ��̼��Ƶ����������Ƕ��٣�
��3����Ӧ���ɵĶ�����̼�������Ƕ��٣�
���� ��һ�κ͵ڶ��μ���25g���ᶼ�Ǽ�����6g��Ҳ���Ƿ�Ӧ��6g̼��ƣ���������ֻ������5.2g��˵��̼����Ѿ���ȫ��Ӧ�����Լ�������������岻�ټ��٣���n=2.8g�����������̼��Ƶ���������������̼��Ƶ������Ͷ�Ӧ�Ļ�ѧ����ʽ�����������̼�������Լ���Ʒ��̼��Ƶ�����������
��� �⣺
��һ�κ͵ڶ��μ���25g���ᶼ�Ǽ�����6g��Ҳ���Ƿ�Ӧ��6g̼��ƣ���������ֻ������5.2g��˵��̼����Ѿ���ȫ��Ӧ�����Լ�������������岻�ټ��٣���n=2.8g����̼��Ƶ�����Ϊ20g-2.8g=17.2g
�����ɵĶ�����̼������Ϊx
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
17.2g x
$\frac{100}{44}$=$\frac{17.2g}{x}$
x=7.568g
ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ$\frac{17.2g}{20g}$��100%=86%
�𣺣�1���ϱ���n����ֵΪ2.8��
��2��ʯ��ʯ��Ʒ��̼��Ƶ�����������86%��
��3����Ӧ���ɵĶ�����̼��������7.568g��
���� ���ݻ�ѧ����ʽ����ʱ����һҪ��ȷ��д��ѧ����ʽ���ڶ�Ҫʹ����ȷ�����ݣ������������Ҫ������

 ��������ϵ�д�
��������ϵ�д�����֪ʶ�����������У��д����һ����
A�����ӵķ��� | B����ѧ�����еġ����� |
�����ᴿ�����ܽ⡢���ˡ����� ľ̿���л������۩����ô������� ��ȥ�����е���������ͨ�����ȵ�ͭ�� | ����ʯȼ�ϩ���ú����Ȼ����ʯ�� ���ֺ�ɫ�����敏������ͭ���������̡����������� ����ϳɲ��ϩ������ϡ��ϳ���ά�ͺϳ��� |
C��ʵ�鰲ȫע������ | D���ճ����ʵ����� |
��ȡ���婁���ȼ��װ�õ������� ������Ȼ��й©����Ҫ���������� �ƾ���Ϩ�𩁩��õ�ñ���� | Ӳˮ����ˮ�����ӷ���ˮ������ ���ͺ�ʳ�ש�������ζ ��ë��ά��ϳ���ά�������ա�����ζ |
A. A B. B C. C D. D
| A�� | ������𣬲�Ҫ���ڴ������Ŵ� | |
| B�� | ȼ�ű���ʱ��ӦԶ����Ⱥ�Ϳ�ȼ�� | |
| C�� | ��Ȼ��й©��Ӧ�����رշ��Ų������̻� | |
| D�� | ���ַ�����������Ũʱ��Ӧ��ʪë����ס�ڱǣ�Ѹ������ |
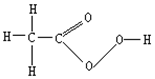 ���������ϸ���Ͳ������и�Ч������ɱ�����ã��ڿ������ǵ��ͷ��ס���ս���б��㷺Ӧ���ڻ�������������ͼΪ�� ������Ľṹʽ�������йع�������������в���ȷ���ǣ�������
���������ϸ���Ͳ������и�Ч������ɱ�����ã��ڿ������ǵ��ͷ��ס���ս���б��㷺Ӧ���ڻ�������������ͼΪ�� ������Ľṹʽ�������йع�������������в���ȷ���ǣ�������| A�� | ����������ӵĻ�ѧʽΪC2H4O3 | B�� | �����������Է�������Ϊ76 | ||
| C�� | ������������Ԫ�ص������������ | D�� | ��ȫȼ������H2O��CO2 |
| A�� | �������� | B�� | ʳ��ù�� | C�� | ƻ��ե֭ | D�� | ľ��ȼ�� |
| A�� |  ���������� | B�� |  �㵹Һ�� | ||
| C�� |  ���������� | D�� |  ���Թ��еμ�Һ�� |