题目内容
10.(1)用一定量液体物质除要量筒外,还需要的仪器有胶头滴管;(2)加热液体物质时,为使其均匀受热,烧杯应放在石棉网上加热;
(3)小明同学用托盘天平称了5.4g NaCl(1g以下用游码),结果老师检查发现他把药品和砝码的位置颠倒了,他称得NaCl的实际质量为4.6.
分析 (1)胶头滴管是取用少量液体时使用的一种仪器,在用量筒量取一定量液体时,向量筒内倒入液体接近所要量取的体积后,改用胶头滴管逐滴加入,以防止继续倒入液体,体积超过所量取值;
(2)烧杯底面积较大,加热时易因受热不均匀而爆裂,所以在使用烧杯进行加热时要垫上石棉网;
(3)正确使用托盘天平称量物品质量时,物品质量=砝码质量+游码质量,如果物品与砝码放反位置,则物品质量=砝码质量-游码质量.
解答 解:(1)量取一定量液体时,除要使用量筒,为准确量取还需要使用胶头滴管;
(2)为使烧杯受热均匀,对烧杯加热时要垫上石棉网,防止受热不匀而炸裂;
(3)使用托盘天平称取5.4gNaCl时,根据题意,砝码使用的为5g砝码,游码质量为0.4g,而当砝码与药品的位置颠倒了,则药品质量=5g-0.4g=4.6g.
故答案为:胶头滴管;石棉网;4.6.
点评 根据托盘天平的构造,天平左端质量=天平右端质量+游码质量,左端放置药品、右端放置砝码时,药品质量=砝码质量+游码质量;左端放置砝码、右端放置药品时,砝码质量=药品质量+游码质量.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
1.据报道,美味龙虾导致“肌溶解“,医生怀疑“洗虾粉“是病因.用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠(Na2SO3)等物质,可能对人体的健康产生危害.Na2SO3中S元素的化合价为( )
| A. | +6 | B. | +4 | C. | +2 | D. | -2 |
15.小明对溶液的下列认识正确的是( )
| A. | 洗涤剂清洗餐具上的油污属于溶解现象 | |
| B. | 天然湖泊中鱼类能生存,表明气体也可溶于水 | |
| C. | 配制溶液时,只要计算正确,所配制溶液的质量分数就不会出现误差 | |
| D. | 溶质在溶液中的分散颗粒都是离子 |
2.图1是元素周期表中铝元素的部分信息,图2是铝原子的结构示意图.下列说法正确的是( )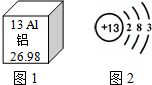

| A. | 铝元素原子核内的中子数为13 | |
| B. | 铝的相对原子质量为26.98 g | |
| C. | 铝离子的核外电子分三层排布 | |
| D. | 铝元素的化学性质与铝原子的最外层电子数有密切的关系 |
19.下列元素符号中都表示金属元素的组是( )
| A. | Hg Ba Mn | B. | Fe He Mg | C. | Ca Na N | D. | H C O |
20.下列物质间的转化可以实现的是( )
| A. | Cu$\stackrel{稀H_{2}SO_{4}}{→}$CuSO4 | B. | CaCO3$\stackrel{稀HCl}{→}$CO2 | ||
| C. | Fe$\stackrel{稀HCl}{→}$FeCl3 | D. | NaNO3$\stackrel{KCl}{→}$NaCl |