题目内容
某铁样品1.1g在纯氧中完全燃烧,得到0.0132gCO2,求此铁样品中碳的质量分数,并判断此样品属于生铁还是钢?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据生成的二氧化碳气体质量,由反应的化学方程式计算出产生样品中碳的质量,进而计算出样品中碳的质量分数;结合生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,进行分析解答.
解答:解:设样品中碳的质量为x,
C+O2
CO2
12 44
x 0.0132g
=
x=0.0036g
×100%≈0.033%.
0.03%<0.033%<2%,该样品属于钢.
答:铁样品中碳的质量分数为0.033%;该样品属于钢.
C+O2
| ||
12 44
x 0.0132g
| 12 |
| 44 |
| x |
| 0.0132g |
| 0.0036g |
| 1.1g |
0.03%<0.033%<2%,该样品属于钢.
答:铁样品中碳的质量分数为0.033%;该样品属于钢.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列有关物质燃烧现象的叙述中,正确的是( )
| A、硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体 |
| B、铁丝在氧气中燃烧:火星四射,生成红色固体 |
| C、镁条在空气中燃烧:发出耀眼的白光,只生成一种黑色固体 |
| D、铁与硫酸铜溶液反应后,溶液由浅绿色变成蓝色 |
往如图所示的烧杯中加入一种物质,轻轻搅拌后,粘在烧杯底部的塑料片脱落,加入的物质可能是( )

| A、硝酸铵 | B、氢氧化钠 |
| C、冰 | D、氯化钠 |
下表中列出了几种物质的熔点,据此判断以下说法正确的是( )
| 物质名称 | 汞 | 金 | 铜 | 铁 | 钨 | 氧气 |
| 沸点/℃ | 356.6 | 2807 | 2595 | 2750 | 5555 | __ 183 |
| 熔点/℃ | -38.3 | 1064 | 1083 | 1535 | 3410 | -218 |
| A、铜掉入铁水中不会熔化 |
| B、在-216℃时,氧气是固态 |
| C、水银温度计可测量-40℃的温度 |
| D、铜与金可熔合成合金 |
下列有关高炉炼铁的说法正确的一组是( )
①高炉中焦炭的作用是产生一氧化碳
②高炉中焦炭的作用是供热
③高炉中把铁矿石冶炼成铁的主要反应原理是2Fe2O3+3C
4Fe+3CO2↑
④高炉炼铁原料有铁矿石、焦炭、石灰石.
①高炉中焦炭的作用是产生一氧化碳
②高炉中焦炭的作用是供热
③高炉中把铁矿石冶炼成铁的主要反应原理是2Fe2O3+3C
| ||
④高炉炼铁原料有铁矿石、焦炭、石灰石.
| A、①②③ | B、②③④ |
| C、①③④ | D、①②④ |
下列化学实验基本操作中正确的是( )
A、 |
B、 |
C、 |
D、 |


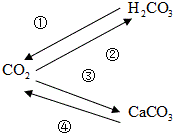 请写出实现下列转化的四个反应的化学方程式:
请写出实现下列转化的四个反应的化学方程式: