题目内容
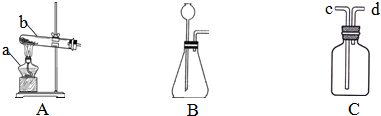
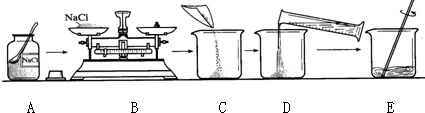
家中的铁锅长时间不用会生锈,钢铁生锈实际是铁与空气中的氧气、 发生化学反应.铁制品生锈可用10%的稀盐酸来除锈,实验室若要配制该盐酸200g,则需用量筒量取溶质质量分数为38%的浓盐酸(密度为1.19g/mL) mL(计算结果保留至0.1);实验室在配制10%的稀盐酸的过程中,除了用到量筒、胶头滴管外,还需要用到的仪器有 、 .
考点:金属锈蚀的条件及其防护,一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度,金属与金属材料
分析:根据铁生锈的条件及稀释前后溶液中的溶质质量不变解答.
解答:解:
钢铁生锈实际是铁与空气中的氧气、水发生化学反应;
实验室若要配制10%盐酸200g,设需用量筒量取溶质质量分数为38%的浓盐酸(密度为1.19g/mL)的体积为x.
根据稀释前后溶液中的溶质质量不变有:
200g×10%=1.19g/mL×x×38%,
解得:X=44.2 mL.
实验室在配制10%的稀盐酸的过程中,除了用到量筒、胶头滴管外,还需要用到的仪器有烧杯、玻璃棒.
答案:
水 44.2 烧杯、玻璃棒.
钢铁生锈实际是铁与空气中的氧气、水发生化学反应;
实验室若要配制10%盐酸200g,设需用量筒量取溶质质量分数为38%的浓盐酸(密度为1.19g/mL)的体积为x.
根据稀释前后溶液中的溶质质量不变有:
200g×10%=1.19g/mL×x×38%,
解得:X=44.2 mL.
实验室在配制10%的稀盐酸的过程中,除了用到量筒、胶头滴管外,还需要用到的仪器有烧杯、玻璃棒.
答案:
水 44.2 烧杯、玻璃棒.
点评:此题考查了多个化学知识点,很多都是贴近生活实际的,体现了化学学以致用的理念,是一道很好的试题.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列关于中和反应的叙述中,正确的是( )
| A、生成盐和水的反应就是中和反应 |
| B、中和反应一定是复分解反应 |
| C、中和反应中溶液的pH一定不变 |
| D、中和反应的生成物一定都是溶于水 |