题目内容
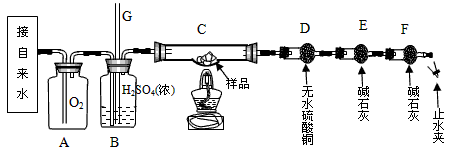
某兴趣小组利用下图装置探究制取气体的原理、方法及性质.结合装置图,回答问题:
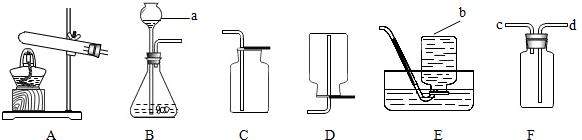
(1)写出图中标号仪器的名称:a
(2)实验室用排水法收集O2,当看到
(3)如果改用F装置收集O2,证明已经收集满O2的方法是将
(4)在B中用块状石灰石与过量稀盐酸充分反应后,过滤反应后的混合物,并向40g滤液中逐滴滴入碳酸钠溶液,同时用pH数字探测仪连续监测,得到如下图图1的曲线:(已知:CaCl2溶液呈中性)
①CD段所对应溶液中含有的阴离子主要是
②BC段的反应生成了白色沉淀,写出该反应的化学方程式,并根据图2选择合适的数据计算所用碳酸钠溶液的溶质质量分数.(写出计算过程)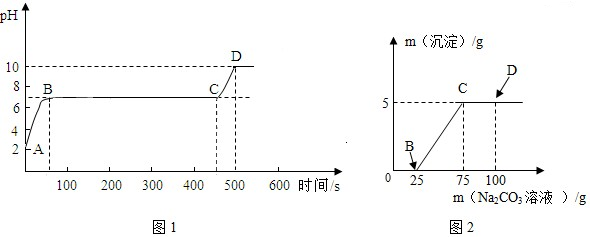

(1)写出图中标号仪器的名称:a
长颈漏斗
长颈漏斗
,b集气瓶
集气瓶
.(2)实验室用排水法收集O2,当看到
瓶口有气泡产生
瓶口有气泡产生
时认为b中集满了O2,后续操作是在水下用玻璃片(粗糙一片)盖住瓶口
在水下用玻璃片(粗糙一片)盖住瓶口
,然后将b从E中取出后正放于实验桌上,发现盖好的玻璃片很容易滑动,原因是集气瓶内气压大于外界大气压
集气瓶内气压大于外界大气压
.(3)如果改用F装置收集O2,证明已经收集满O2的方法是将
带火星
带火星
的木条放在c
c
导管口(选“c”或“d”),观察是否复燃;(4)在B中用块状石灰石与过量稀盐酸充分反应后,过滤反应后的混合物,并向40g滤液中逐滴滴入碳酸钠溶液,同时用pH数字探测仪连续监测,得到如下图图1的曲线:(已知:CaCl2溶液呈中性)
①CD段所对应溶液中含有的阴离子主要是
CO32ˉ、Clˉ
CO32ˉ、Clˉ
.②BC段的反应生成了白色沉淀,写出该反应的化学方程式,并根据图2选择合适的数据计算所用碳酸钠溶液的溶质质量分数.(写出计算过程)

分析:(1)根据装置中所指定仪器的图示,写出该仪器的名称;
(2)实验室用排水法收集O2,当看到瓶口有气泡产生时,说明水被排了了,气体收集满;为防止气体的溢出,应该在水下用玻璃片(粗糙一片)盖住瓶口;根据气压分析;
(3)验满氧气用带火星的木条,收集时根据氧气的密度比空气大,从长管进入,空气从短管排出;
(4)①根据盐酸过量,所以滤液中有盐酸和氯化钙,逐滴滴入碳酸钠,AB段是碳酸钠和过量的盐酸反应,BC段是碳酸钠和氯化钙反应产生碳酸钙沉淀,CD段是碳酸钠过量,溶液显碱性;②根据BC段是碳酸钠和氯化钙反应产生的沉淀计算碳酸钠的质量,再根据溶质质量分数的公式计算出碳酸钠的质量分数.
(2)实验室用排水法收集O2,当看到瓶口有气泡产生时,说明水被排了了,气体收集满;为防止气体的溢出,应该在水下用玻璃片(粗糙一片)盖住瓶口;根据气压分析;
(3)验满氧气用带火星的木条,收集时根据氧气的密度比空气大,从长管进入,空气从短管排出;
(4)①根据盐酸过量,所以滤液中有盐酸和氯化钙,逐滴滴入碳酸钠,AB段是碳酸钠和过量的盐酸反应,BC段是碳酸钠和氯化钙反应产生碳酸钙沉淀,CD段是碳酸钠过量,溶液显碱性;②根据BC段是碳酸钠和氯化钙反应产生的沉淀计算碳酸钠的质量,再根据溶质质量分数的公式计算出碳酸钠的质量分数.
解答:解:(1)a是长颈漏斗 b是集气瓶;
(2)实验室用排水法收集O2,当看到瓶口有气泡产生时,说明水被排了了,气体收集满;为防止气体的溢出,应该在水下用玻璃片(粗糙一片)盖住瓶口;因为收集满氧气的集气瓶内的气压大于外界大气压,所以发现盖好的玻璃片很容易滑动;
(3)验满氧气用带火星的木条放在集气瓶口看是否复燃,用该装置收集时根据氧气的密度比空气大,氧气从长管进入,空气从短管排出,到收集满时,氧气就会从c管排出,故带火星的木条应该放在c导管口,看是否复燃;
(4)①CD段溶液显碱性,是碳酸钠过量,故含有碳酸根离子(CO32ˉ),碳酸钠和过量的盐酸、氯化钙反应均产生氯化钠,故溶液中一定含有氯离子(Clˉ);
②段是碳酸钠和氯化钙完全反应产生了 5g碳酸钙沉淀可以计算碳酸钠的质量,再根据溶质质量分数的公式计算出碳酸钠的质量分数.
解:设生成 5g碳酸钙需要碳酸钠的质量为X
CaCl2+Na2CO3═2NaCl+CaCO3↓
106 100
X 5g
=
∴X=5.3g
碳酸钠的质量分数=
×100%=10.6%
答:所用碳酸钠溶液的溶质质量分数为10.6%.
故答案为:(1)a是长颈漏斗 b是集气瓶
(2)瓶口有气泡产生;在水下用玻璃片(粗糙面)盖住瓶口;集气瓶内气压大于外界大气压
(3)带火星;c
(4)①CO32ˉ、Clˉ
②解:设生成 5g碳酸钙需要碳酸钠的质量为X
CaCl2+Na2CO3═2NaCl+CaCO3↓
106 100
X 5g
=
∴X=5.3g
碳酸钠的质量分数=
×100%=10.6%
答:所用碳酸钠溶液的溶质质量分数为10.6%.
(2)实验室用排水法收集O2,当看到瓶口有气泡产生时,说明水被排了了,气体收集满;为防止气体的溢出,应该在水下用玻璃片(粗糙一片)盖住瓶口;因为收集满氧气的集气瓶内的气压大于外界大气压,所以发现盖好的玻璃片很容易滑动;
(3)验满氧气用带火星的木条放在集气瓶口看是否复燃,用该装置收集时根据氧气的密度比空气大,氧气从长管进入,空气从短管排出,到收集满时,氧气就会从c管排出,故带火星的木条应该放在c导管口,看是否复燃;
(4)①CD段溶液显碱性,是碳酸钠过量,故含有碳酸根离子(CO32ˉ),碳酸钠和过量的盐酸、氯化钙反应均产生氯化钠,故溶液中一定含有氯离子(Clˉ);
②段是碳酸钠和氯化钙完全反应产生了 5g碳酸钙沉淀可以计算碳酸钠的质量,再根据溶质质量分数的公式计算出碳酸钠的质量分数.
解:设生成 5g碳酸钙需要碳酸钠的质量为X
CaCl2+Na2CO3═2NaCl+CaCO3↓
106 100
X 5g
| 106 |
| X |
| 100 |
| 5g |
碳酸钠的质量分数=
| 5.3g |
| 75g-25g |
答:所用碳酸钠溶液的溶质质量分数为10.6%.
故答案为:(1)a是长颈漏斗 b是集气瓶
(2)瓶口有气泡产生;在水下用玻璃片(粗糙面)盖住瓶口;集气瓶内气压大于外界大气压
(3)带火星;c
(4)①CO32ˉ、Clˉ
②解:设生成 5g碳酸钙需要碳酸钠的质量为X
CaCl2+Na2CO3═2NaCl+CaCO3↓
106 100
X 5g
| 106 |
| X |
| 100 |
| 5g |
碳酸钠的质量分数=
| 5.3g |
| 75g-25g |
答:所用碳酸钠溶液的溶质质量分数为10.6%.
点评:本题虽然是有关气体的制取,但考查的重点是有关操作注意事项的细节考查,也是学生实验操作能力的体现;计算题关键是能够读准坐标中每一段的含义.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某兴趣小组利用废旧电话线中的金属铜丝进行了如下一系列实验.
(1)如图所示,将铜丝分别放入盛有氯化锌溶液、稀硫酸、硝酸银溶液的试管中,观察到的现象是________,发生反应的化学方程式是________.

(2)用细线吊着的长玻璃棒的两端分别绕有40 cm长的铜丝(如右图所示),使玻璃棒保持平衡,用酒精灯加热玻璃棒左端2分钟后冷却,可以观察到的现象是________,产生该现象的原因是________.

(3)将四段相同长度的铜丝分别按下图所示放置一个月,观察并记录现象如下
| E | F | G | H | |
| 实 验 装 置 |  |  |  |  |
| 实验现象 | 铜丝不生锈 | 铜 丝 不 生 锈 | 铜丝不生锈 | 铜丝生锈 |
结论:铜生锈是铜与________共同作用的结果.
燃烧是一种发光、发热的剧烈的化学反应.认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的.
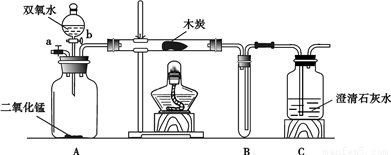
已知木炭是一种可燃物.某化学兴趣小组利用下图所示实验装置验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧.
该装置气密性良好.请按下列实验步骤完成探究活动,要求实验过程中不得拆、装仪器.
(1)步骤Ⅱ中,木炭不燃烧的原因是______.
(2)步骤Ⅲ中,装置B的作用是______.
(3)步骤Ⅳ的操作是______、______,观察现象.
(4)步骤Ⅴ产生的现象是木炭燃烧发出白光并放出热量、______.
(5)装置A中发生反应的化学方程式为______ 2H2O+O2↑

已知木炭是一种可燃物.某化学兴趣小组利用下图所示实验装置验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧.
该装置气密性良好.请按下列实验步骤完成探究活动,要求实验过程中不得拆、装仪器.
| 步骤 | 操作 |
| Ⅰ | 打开活塞a,缓缓通入氮气一段时间后关闭a |
| Ⅱ | 点燃酒精灯,观察现象 |
| Ⅲ | 盖灭酒精灯,待仪器恢复到常温 |
| Ⅳ | … |
| Ⅴ | 点燃酒精灯,观察现象 |
| … | … |
(2)步骤Ⅲ中,装置B的作用是______.
(3)步骤Ⅳ的操作是______、______,观察现象.
(4)步骤Ⅴ产生的现象是木炭燃烧发出白光并放出热量、______.
(5)装置A中发生反应的化学方程式为______ 2H2O+O2↑