题目内容
现有Na2CO3和Na2SO4的固体混合物样品共12g,将其溶解于92.4g水中,向所得溶液中逐滴滴加H2SO4溶液,加入H2SO4溶液的质量与产生气体的质量的关系如图所示.求:
(1)固体混合物中Na2CO3的质量.
(2)求样品与H2SO4溶液恰好完全反应后所得Na2SO4溶液中溶质的质量分数.
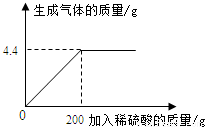
【答案】分析:分析知Na2CO3和Na2SO4中只有碳酸钠能与稀硫酸反应,且依据图象可知反应完全后生成的二氧化碳质量是4.4g,所以依据方程式据二氧化碳的质量可求碳酸钠和生成的硫酸钠质量,据此分析解答即可;
解答:解:依据图象可知完全反应后生成的二氧化碳的质量是4.4g
设固体混合物中Na2CO3的质量的质量为x,反应中生成Na2SO4的质量为y.
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 142 44
x y 4.4g
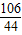 =
=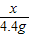 =
=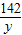
x=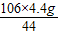 =10.6g
=10.6g
y=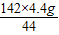 =14.2g
=14.2g
所得Na2SO4溶液中溶质的质量分数为: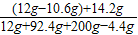 ×100%=5.2%
×100%=5.2%
答:(1)固体混合物中Na2CO3的质量为10.6g.
(2)样品与硫酸溶液恰好完全反应后所得Na2SO4溶液中溶质的质量分数为5.2%.
点评:此题是对化学方程式计算的题目,解题的关键是能够依据图象得到二氧化碳的质量是4.4g,然后依据化学方程式进行计算即可.
解答:解:依据图象可知完全反应后生成的二氧化碳的质量是4.4g
设固体混合物中Na2CO3的质量的质量为x,反应中生成Na2SO4的质量为y.
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 142 44
x y 4.4g
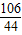 =
=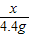 =
=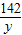
x=
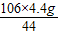 =10.6g
=10.6g y=
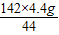 =14.2g
=14.2g所得Na2SO4溶液中溶质的质量分数为:
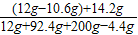 ×100%=5.2%
×100%=5.2% 答:(1)固体混合物中Na2CO3的质量为10.6g.
(2)样品与硫酸溶液恰好完全反应后所得Na2SO4溶液中溶质的质量分数为5.2%.
点评:此题是对化学方程式计算的题目,解题的关键是能够依据图象得到二氧化碳的质量是4.4g,然后依据化学方程式进行计算即可.

练习册系列答案
 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
![]()
现有由海水晒得的粗盐,其中含有CaCl2和MgCl2两种杂质。某活动小组将粗盐溶于水后设计了两种除去粗盐中杂质的方法,所用到的试剂均为A、NaOH溶液;B、Na2CO3溶液;C、稀盐酸,除杂的两种方法如下:
请回答:
(1)方法一的滤液③中含有的溶质分别为 (用化学式表示)
(2)方法二的滤液③中含有的溶质分别为 (用化学式表示)
(3)根据两种固体M、N的成分分析哪一种方法合理 。

 (2011?盂县一模)现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质,存在如图所示的相互反应和转化关系,图中“-”表示两端的物质间可以发生化学反应,“→”表示物质间存在相应的转化关系,回答下列问题:
(2011?盂县一模)现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质,存在如图所示的相互反应和转化关系,图中“-”表示两端的物质间可以发生化学反应,“→”表示物质间存在相应的转化关系,回答下列问题:
