题目内容
已知4.8g金属M与足量的稀硫酸反应,生成MSO4和0.4g氢气,则M的相对原子质量为.
【答案】分析:根据题设给出的生成盐的化学式,完成金属与硫酸反应的化学方程式,然后根据反应的化学方程式,由金属与生成氢气的质量关系,计算出金属的相对原子质量.
解答:解:设金属M的相对原子质量为m
M+H2SO4═MSO4+H2↑
m 2
4.8g 0.4g
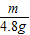 =
=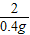 m=24
m=24
故答案为:24.
点评:根据化学方程式的计算,反应的化学方程式是计算的基本,此题在书写反应的化学方程式上需要留意.
解答:解:设金属M的相对原子质量为m
M+H2SO4═MSO4+H2↑
m 2
4.8g 0.4g
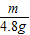 =
=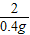 m=24
m=24故答案为:24.
点评:根据化学方程式的计算,反应的化学方程式是计算的基本,此题在书写反应的化学方程式上需要留意.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目