题目内容
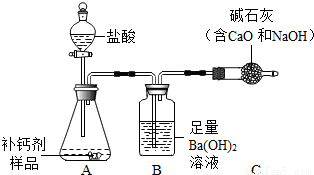
某兴趣小组利用如图装置(夹持装置略去),测定某种补钙剂中碳酸钙的含量.[查得资料]
①该补钙剂的主要成分是碳酸钙,其他成分遇到盐酸时无气体生成.
②二氧化碳通入足量的氢氧化钡溶液中,会生成白色碳酸钡沉淀:Ba(OH)2+CO2═BaCO3↓+H2O.
[测定方法]
通过测定B装置中产生沉淀的质量,以确定碳酸钙的质量分数.
(1)碳酸钙属于 (填“酸”“碱”或“盐”).
[进行实验]
实验过程中,装置气密性良好.取适量的该补钙剂样品进行实验.
(2)观察到:A装置中 ,固体逐渐溶解;B装置中产生白色沉淀.
(3)从A装置中导出的气体除了二氧化碳和水蒸气外,还含有氯化氢.请写出氢氧化钡溶液与氯化氢气体反应的化学方程式: .
[交流讨论]
通过小组讨论提出改进实验装置的措施:在A、B装置之间增加洗气装置,以除去氯化氢气体.
(4)经改进后,实验测得B装置中沉淀的质量偏小.试分析其可能的一种原因: .
(5)C装置的作用是 .
【答案】分析:[测定方法](1)根据物质的分类方法来完成解答;
[进行实验](2)碳酸钙可以和稀盐酸反应生成二氧化碳,可以据此解答;
(3)氯化氢和氢氧化钡溶液反应生成了氯化钡和水,可以据此写出该反应的化学方程式;
[交流讨论](4)锥形瓶A中的气体不能全部进入B装置中,所以会导致测量结果偏低,可依据此解答;
(5)空气中有二氧化碳,C装置可以有效的防止空气中的二氧化碳进入B装置中,可以据此解答.
解答:解:[测定方法](1)根据物质的分类可以知道碳酸钙由酸根离子和金属离子构成的,所以属于盐类;
[进行实验](2)碳酸钙可以和稀盐酸反应生成二氧化碳,所以能够观察A中有气泡冒出;
(3)氯化氢和氢氧化钡溶液反应生成了氯化钡和水,该反应的化学方程式为Ba(OH)2+2HCl═BaCl2+2H2O;
[交流讨论](4)反应生成的二氧化碳没有全部被吸收或是锥形瓶A中的气体不能全部进入B装置中,都会导致测量结果偏低;
(5)空气中有二氧化碳,C装置可以有效的防止空气中的二氧化碳进入B装置中,从而使减小测量误差.
故答案为:(1)盐;
(2)有大量气泡产生;
(3)Ba(OH)2+2HCl═BaCl2+2H2O;
(4)反应生成的CO2没有被氢氧化钡溶液全部吸收(或锥形瓶中残留CO2等);
(5)防止空气中的CO2进入装置B中.
点评:在对盐的性质的探究过程中,根据物质的化学性质,要认真分析,要把握实验设计的每一个步骤中的实验目的,并能够要分析数据的误差.本考点经常出现在实验题中.
[进行实验](2)碳酸钙可以和稀盐酸反应生成二氧化碳,可以据此解答;
(3)氯化氢和氢氧化钡溶液反应生成了氯化钡和水,可以据此写出该反应的化学方程式;
[交流讨论](4)锥形瓶A中的气体不能全部进入B装置中,所以会导致测量结果偏低,可依据此解答;
(5)空气中有二氧化碳,C装置可以有效的防止空气中的二氧化碳进入B装置中,可以据此解答.
解答:解:[测定方法](1)根据物质的分类可以知道碳酸钙由酸根离子和金属离子构成的,所以属于盐类;
[进行实验](2)碳酸钙可以和稀盐酸反应生成二氧化碳,所以能够观察A中有气泡冒出;
(3)氯化氢和氢氧化钡溶液反应生成了氯化钡和水,该反应的化学方程式为Ba(OH)2+2HCl═BaCl2+2H2O;
[交流讨论](4)反应生成的二氧化碳没有全部被吸收或是锥形瓶A中的气体不能全部进入B装置中,都会导致测量结果偏低;
(5)空气中有二氧化碳,C装置可以有效的防止空气中的二氧化碳进入B装置中,从而使减小测量误差.
故答案为:(1)盐;
(2)有大量气泡产生;
(3)Ba(OH)2+2HCl═BaCl2+2H2O;
(4)反应生成的CO2没有被氢氧化钡溶液全部吸收(或锥形瓶中残留CO2等);
(5)防止空气中的CO2进入装置B中.
点评:在对盐的性质的探究过程中,根据物质的化学性质,要认真分析,要把握实验设计的每一个步骤中的实验目的,并能够要分析数据的误差.本考点经常出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目