题目内容
下列各组离子在水溶液中能大量共存的是
- A.H+ Ba2+ NO3- OH-
- B.H+ K+ CI- CO32-
- C.Na+ Ag+ NO3- CO32-
- D.Na+ K+ OH- SO42-
D
A、根据氢离子和氢氧根离子会生成水进行分析;
B、根据氢离子和碳酸根离子会生成二氧化碳进行分析;
C、根据碳酸根离子和银离子会生成碳酸银沉淀进行分析;
D、根据四种离子之间不会反应进行分析.
解答:A、氢离子和氢氧根离子会生成水而不能共存,故A错误;
B、氢离子和碳酸根离子会生成二氧化碳和水,不能共存,故B错误;
C、银离子和碳酸根离子会生成碳酸银沉淀而不能共存,故C错误;
D、四种离子之间不会反应,可以共存,故D正确;
故选D.
点评:在解此类题时,首先分析选项中离子的性质,只要会生成沉淀、气体、水中的一种,就不能共存.
A、根据氢离子和氢氧根离子会生成水进行分析;
B、根据氢离子和碳酸根离子会生成二氧化碳进行分析;
C、根据碳酸根离子和银离子会生成碳酸银沉淀进行分析;
D、根据四种离子之间不会反应进行分析.
解答:A、氢离子和氢氧根离子会生成水而不能共存,故A错误;
B、氢离子和碳酸根离子会生成二氧化碳和水,不能共存,故B错误;
C、银离子和碳酸根离子会生成碳酸银沉淀而不能共存,故C错误;
D、四种离子之间不会反应,可以共存,故D正确;
故选D.
点评:在解此类题时,首先分析选项中离子的性质,只要会生成沉淀、气体、水中的一种,就不能共存.

练习册系列答案
相关题目
 构建知识网络是学习和研究化学常用的科学方法.图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法.图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.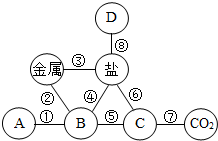 构建知识网络是学习和研究化学常用的科学方法.如图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D表示氧化物、酸、碱、盐的某一种,“-”表示物质之间能够发生化学反应.
构建知识网络是学习和研究化学常用的科学方法.如图是小李同学在复习“我们身边的化学物质”时构建的知识网络,其中A、B、C、D表示氧化物、酸、碱、盐的某一种,“-”表示物质之间能够发生化学反应.