题目内容
加热24.5g KClO3和8.2g MnO2的混合物,反应完全后得到14.9g KCl.根据质量守恒定律,确定生成的氧气的质量为( )
| A、6.7g | B、39.4g |
| C、9.6g | D、17.8g |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,反应前后的质量差即为生成氧气的质量.
解答:解:生成氧气的质量为:24.5g+8.2g-14.9g=17.8g,
故选:D.
故选:D.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
一种元素与其它元素之间最本质的区别是( )不同.
| A、中子数 | B、质子数 |
| C、最外层电子数 | D、核外电子数 |
CO2能使紫色石蕊试液变红是因为( )
| A、密度比空气大 |
| B、可以溶解在水里 |
| C、与水发生化学反应生成碳酸 |
| D、CO2分子可以与紫色石蕊直接反应 |
实验室制取二氧化碳气体时,常用( )
| A、木碳和氧气反应 |
| B、大理石和稀盐酸 |
| C、大理石和稀硫酸 |
| D、煅烧石灰石 |
下列关于实验现象的描述不正确的是( )
| A、红磷在空气中燃烧,产生白色浓烟 |
| B、铁丝在空气中燃烧,火星四射 |
| C、木炭在空气中燃烧,发红光 |
| D、镁在空气中燃烧发出耀眼的白光 |
H2中混有的CO2,最好的方法是( )
| A、将混合气体通过灼热的CuO |
| B、将混合气体通入澄清的石灰水 |
| C、将混合气体通入水中 |
| D、将混合气体通过红热的木炭层 |
下列物质中属于纯净物的是( )
| A、蒸馏水 | B、海水 |
| C、空气 | D、石灰水 |
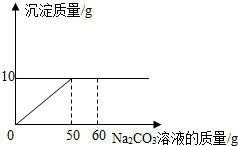 将14.4g含有NaCl和CaCl2的固体混合物,加入到45.6g的足量的水中,在所得溶液中逐滴加入一定定溶质质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量质量与沉淀质量关系如图:(化学方程式 CaCl2+Na2CO3═CaCO3↓+2NaCl)
将14.4g含有NaCl和CaCl2的固体混合物,加入到45.6g的足量的水中,在所得溶液中逐滴加入一定定溶质质量分数的Na2CO3溶液,所加入Na2CO3溶液的质量质量与沉淀质量关系如图:(化学方程式 CaCl2+Na2CO3═CaCO3↓+2NaCl) 2012年6月16日18时37分,“神舟九号飞船”在酒泉卫星发射中心,由长征二号F遥九运载火箭成功发射,准确入轨.
2012年6月16日18时37分,“神舟九号飞船”在酒泉卫星发射中心,由长征二号F遥九运载火箭成功发射,准确入轨.