题目内容
关于自来水的生产说法正确的是( )
A.加入适量液氯去除天然水中的杂质
B.过滤能除去天然水中所有的杂质
C.加入明矾促使微小悬浮杂质的沉降
D.最终得到的自来水属于纯净物
【考点】自来水的生产过程与净化方法;过滤的原理、方法及其应用;纯净物和混合物的判别.
【专题】空气与水.
【分析】A、根据氯气通入水后发生反应生成次氯酸,具有杀菌的作用解答;
B、根据过滤是除去水中不溶性杂质的方法,不能除去所有的杂质解答;
C、根据明矾溶于水形成的胶体具有吸附性,能将水中不溶性固体杂质吸附在其表面形成大颗粒易于沉降解答;
D、根据自来水中含有水和其它矿物质,是混合物解答;
【解答】解:
A、氯气溶于水生成次氯酸,次氯酸能够杀菌消毒,故错;
B、过滤是除去水中不溶性杂质的方法,不能除去所有的杂质,错误;
C、明矾溶于水形成的胶体具有吸附性,能将水中不溶性固体杂质吸附在其表面形成大颗粒易于沉降,正确;
D、自来水中含有水和其它可溶性矿物质,是混合物;故错;
故选:C
【点评】掌握水的净化的方法是正确解答本题的关键.明矾溶于水形成的胶体具有吸附性,过滤是除去水中不溶性杂质的方法.

 阅读快车系列答案
阅读快车系列答案下表是KNO3和NaNO3在不同温度时的溶解度(单位:g/100g水).
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaNO3 | 73 | 80 | 87 | 95 | 103 | 114 | 125 | 136 | 150 | 163 | 170 |
①10℃时,NaNO3的溶解度是 80 g/100g水.
②从表中数据看出KNO3与NaNO3溶解度随温度升高而 (填“增大”或“减小”); 从KNO3饱和溶液中提取KNO3晶体常采用的方法是 .
③20℃时,向100g水中加入35gKNO3,要使其完全溶解,应 (填“升高”或“降低”)溶液温度.
④现有80℃的NaNO3饱和溶液250g,要使其析出晶体70g应降温至 ℃;
⑤KNO3和NaNO3在t℃时的溶解度均为W g/100g水,分析上表可推知,W数值所在的最小范围是 ;现将溶剂质量相同的KNO3和NaNO3的饱和溶液从t1℃降温到t2℃,前者析出的晶体比后者多,则t1、t2的取值范围正确的是 (填字母).
A.仅0≤t2<t1≤t B.仅t≤t2<t1≤100 C.0≤t2<t1≤100 D.0≤t1<t2≤100.

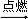 c H2O+d CO2配平后a、b、c、d数值为( )
c H2O+d CO2配平后a、b、c、d数值为( )



 4 NaOH Na2SO4
4 NaOH Na2SO4