题目内容
人类生活离不开金属.
(1)铁是生活中常用的金属.某“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.发热剂需接触到空气才会发热,原因是铁要与 氧气等物质共同作用才会生锈.
(2)CO、C均可和金属氧化物反应,这是因为二者均有 性,木炭与氧化铜反应的化学方程式为 .
(3)应用金属活动性顺序能帮助我们进一步学习金属性质.已知下列各组物质间均能发生置换反应.
A.Cu和AgNO3溶液 B.Mg和MnSO4溶液 C.Mn和盐酸
①写出Cu和AgNO3溶液反应的化学方程式 .
②Mn、Ag、Mg、Cu四种金属的活动性由强到弱的顺序 .
(1)铁是生活中常用的金属.某“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.发热剂需接触到空气才会发热,原因是铁要与
(2)CO、C均可和金属氧化物反应,这是因为二者均有
(3)应用金属活动性顺序能帮助我们进一步学习金属性质.已知下列各组物质间均能发生置换反应.
A.Cu和AgNO3溶液 B.Mg和MnSO4溶液 C.Mn和盐酸
①写出Cu和AgNO3溶液反应的化学方程式
②Mn、Ag、Mg、Cu四种金属的活动性由强到弱的顺序
考点:金属锈蚀的条件及其防护,一氧化碳的化学性质,金属活动性顺序及其应用,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途,金属与金属材料
分析:(1)根据铁制品锈蚀的过程,实际上是铁与空气中的氧气,水蒸气等发生化学反应的过程解答本题.
(2)CO、C都具有还原性;碳还原氧化铜生成铜和二氧化碳,据此写出化学化学方程式.
(3)根据金属与盐的反应规律,利用Cu、Mn、Ag、Mg四种金属及其化合物间可发生的反应,推断Cu、Mn、Ag、Mg四种金属活动性由强至弱的顺序.
(2)CO、C都具有还原性;碳还原氧化铜生成铜和二氧化碳,据此写出化学化学方程式.
(3)根据金属与盐的反应规律,利用Cu、Mn、Ag、Mg四种金属及其化合物间可发生的反应,推断Cu、Mn、Ag、Mg四种金属活动性由强至弱的顺序.
解答:解:(1)根据铁制品锈蚀的过程,实际上是铁与空气中的氧气,水蒸气等发生化学反应的过程,因此发热剂需接触到空气才会发热,原因是铁要与 水、氧气等物质共同作用才会生锈.
故答案为:水.
(2)CO、C均有还原性,所以CO、C均可和金属氧化物反应;木炭与氧化铜反应生成铜和二氧化碳,化学方程式为C+2CuO
2Cu+CO2↑;
故答案为:还原;C+2CuO
2Cu+CO2↑.
(3)①Cu和AgNO3溶液反应生成银和硝酸铜,化学方程式为Cu+2AgNO3═2Ag+Cu(NO3)2;
故填:Cu+2AgNO3═2Ag+Cu(NO3)2;
②根据A.Cu和AgNO3溶液,说明铜的活动性比银强;B.Mg和MnSO4 溶液反应,说明镁的活动性比锰强;则Cu、Mn、Ag、Mg四种金属活动性由强至弱的顺序为Mg、Mn、Cu、Ag.
故答案为:Mg、Mn、Cu、Ag.
故答案为:水.
(2)CO、C均有还原性,所以CO、C均可和金属氧化物反应;木炭与氧化铜反应生成铜和二氧化碳,化学方程式为C+2CuO
| ||
故答案为:还原;C+2CuO
| ||
(3)①Cu和AgNO3溶液反应生成银和硝酸铜,化学方程式为Cu+2AgNO3═2Ag+Cu(NO3)2;
故填:Cu+2AgNO3═2Ag+Cu(NO3)2;
②根据A.Cu和AgNO3溶液,说明铜的活动性比银强;B.Mg和MnSO4 溶液反应,说明镁的活动性比锰强;则Cu、Mn、Ag、Mg四种金属活动性由强至弱的顺序为Mg、Mn、Cu、Ag.
故答案为:Mg、Mn、Cu、Ag.
点评:本题考查了金属的性质以及有关反应的化学方程式的书写问题,完成此题,要熟悉金属活动性强弱以及常见化学反应式的书写.

练习册系列答案
相关题目
2013年11月23日,在华沙气候大会上,中国代表团提出的要坚定不移地走绿色低碳发展之路而备受关注.下列不符合低碳理念的是( )
| A、积极发展太阳能产业 |
| B、营造森林绿地 |
| C、出门以步代车 |
| D、焚烧落叶 |
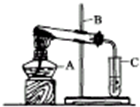 如图是用木炭粉还原氧化铜的装置图.
如图是用木炭粉还原氧化铜的装置图. 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.