题目内容
填空题:
①已知HnRO2n的相对分子质量为A,则R的相对原子质量为
②某氧化物含氧元素的质量分数为20%,已知每个分子中有2个氧原子.该氧化物的相对分子质量是
③下列含氮化合物中,氮元素化合价由高到低的排列顺序是
①硫酸铵②硝酸③氮气④二氧化氮⑤三氧化二氮 ⑥一氧化氮
④过滤操作所用到的玻璃仪器有
⑤1996年,科学家在宇宙深处发现了H3+和H3分子,1个H3+离子中含有
①已知HnRO2n的相对分子质量为A,则R的相对原子质量为
A-33n
A-33n
.②某氧化物含氧元素的质量分数为20%,已知每个分子中有2个氧原子.该氧化物的相对分子质量是
160
160
.③下列含氮化合物中,氮元素化合价由高到低的排列顺序是
②④⑤⑥③①
②④⑤⑥③①
.①硫酸铵②硝酸③氮气④二氧化氮⑤三氧化二氮 ⑥一氧化氮
④过滤操作所用到的玻璃仪器有
玻璃棒、烧杯、漏斗
玻璃棒、烧杯、漏斗
.⑤1996年,科学家在宇宙深处发现了H3+和H3分子,1个H3+离子中含有
3
3
个质子和2
2
个电子.H3属于单质
单质
(填混合物,单质,或化合物)分析:①相对分子质量为构成分子的各原子的相对原子质量之和;
②根据化合物组成元素质量分数=
×100%分析;
③根据在化合物中正负化合价代数和为零,结合各选项中的化学式进行解答本题.
④根据过滤操作的原理、使用的仪器进行分析解答;
⑤元素符号右下角的数字表示1个分子或原子团中所含某种原子的个数.在原子中核内质子数等于核外电子数.阳离子是失去电子形成的.所带电荷数就是失去电子的数目.纯净物只含一种成分,单质是同种元素组成的纯净物.
②根据化合物组成元素质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
③根据在化合物中正负化合价代数和为零,结合各选项中的化学式进行解答本题.
④根据过滤操作的原理、使用的仪器进行分析解答;
⑤元素符号右下角的数字表示1个分子或原子团中所含某种原子的个数.在原子中核内质子数等于核外电子数.阳离子是失去电子形成的.所带电荷数就是失去电子的数目.纯净物只含一种成分,单质是同种元素组成的纯净物.
解答:解:①某化合物的化学式为HnRO2n,已知其式量是A,设R的相对原子质量为x,则1×n+x+16×2n=A,则x=A-33n.
②由题意得,该氧化物含氧元素的质量分数为
×100%=20%,所以该氧化物的相对分子质量是160
③根据在化合物中正负化合价代数和为零,①硫酸铵中氮元素的化合价为-3价,②硝酸中氮元素的化合价为+5价,③氮气中氮元素的化合价为0价,④二氧化氮中氮元素的化合价为+4价,⑤三氧化二氮中氮元素的化合价为+3价,⑥一氧化氮中氮元素的化合价为+2价,
氮元素化合价由高到低的排列顺序是②④⑤⑥③①
④过滤操用到的仪器有铁架台、漏斗、烧杯、玻璃棒等;其中属于玻璃仪器有:漏斗、烧杯、玻璃棒.
⑤1个H3+含有3个氢原子,并带有1个单位的正电荷.1个氢原子含有1个质子和1个电子,因此3个氢原子带有3个质子和3个电子;由于带有1个单位的正电荷,说明失去了1个电子,因此1个H3+共带有3个质子和2个电子;H3中只含H3一种分子,因此H3属于纯净物;H3只由氢元素组成,不再含有其它元素,因此H3属于单质.
故答案为:①.A-33n
②.160
③.②④⑤⑥③①
④.玻璃棒、烧杯、漏斗
⑤.3;2; 单质
②由题意得,该氧化物含氧元素的质量分数为
| 16×2 |
| 该氧化物的相对分子质量 |
③根据在化合物中正负化合价代数和为零,①硫酸铵中氮元素的化合价为-3价,②硝酸中氮元素的化合价为+5价,③氮气中氮元素的化合价为0价,④二氧化氮中氮元素的化合价为+4价,⑤三氧化二氮中氮元素的化合价为+3价,⑥一氧化氮中氮元素的化合价为+2价,
氮元素化合价由高到低的排列顺序是②④⑤⑥③①
④过滤操用到的仪器有铁架台、漏斗、烧杯、玻璃棒等;其中属于玻璃仪器有:漏斗、烧杯、玻璃棒.
⑤1个H3+含有3个氢原子,并带有1个单位的正电荷.1个氢原子含有1个质子和1个电子,因此3个氢原子带有3个质子和3个电子;由于带有1个单位的正电荷,说明失去了1个电子,因此1个H3+共带有3个质子和2个电子;H3中只含H3一种分子,因此H3属于纯净物;H3只由氢元素组成,不再含有其它元素,因此H3属于单质.
故答案为:①.A-33n
②.160
③.②④⑤⑥③①
④.玻璃棒、烧杯、漏斗
⑤.3;2; 单质
点评:本题难度不大,考查同学们结合信息、灵活运用化学式的含义与有关计算进行、化合价的求解、过滤操作、单质的定义来分析问题,解决问题的能力.

练习册系列答案
相关题目
某化学课外兴趣小组探究氢气还原氧化铜的反应,有如下实验装置:
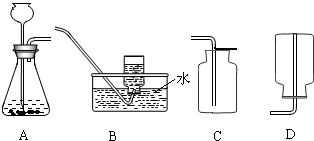
(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳
的化学方程式 ; ;
上述可用于收集二氧化碳装置是 (用装置字母序号填空).
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三: (请补充完成假设三).
②实验探究:(填写表中空格)
③数据处理:甲同学称取Wg红色固体加入到足量硫酸溶液中使其充分反应后, (填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算,若m
g(选填>、<或=),则假设二成立;若m
g(选填>、<或=),则假设三成立.
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.

(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳
的化学方程式
上述可用于收集二氧化碳装置是
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:
②实验探究:(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设 |
| b.取少量红色固体加入到足量硫酸溶液中 | 假设二和假设三均成立 |
| 64W |
| 144 |
| 64W |
| 144 |
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.

 ,则 ,其化学式为 ▲ ,其碳、氢和氧元素的最
,则 ,其化学式为 ▲ ,其碳、氢和氧元素的最