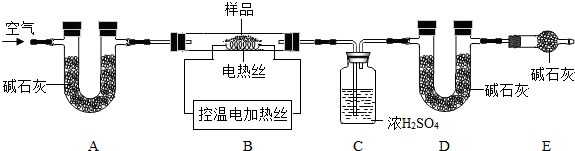
题目内容
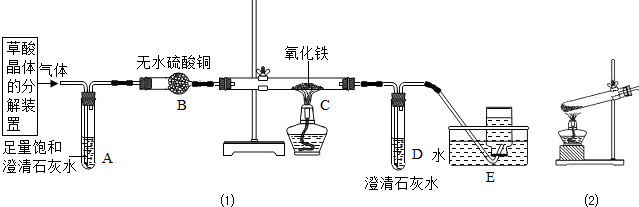
(1)某实验小组在研究二氧化碳的性质时,根据下图进行实验.请回答:A中的现象是______,B中反应的化学方程式是______.(2)该小组利用对比的方法研究二氧化硫的性质,进行如下探究.
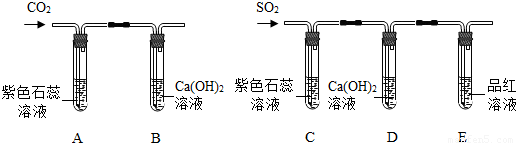
[提出问题]二氧化硫与二氧化碳均属于非金属氧化物,是否具有相似的化学性质呢?
[查阅资料]二氧化硫具有漂白性,其原因是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,实验室常用红色的品红溶液检验二氧化硫的存在.
[实验探究]实验装置如图所示.
①装置C中紫色石蕊溶液变红,是由于二 氧化硫与水反应生成了亚硫酸(H2SO3);装置D中澄清石灰水变浑浊,该反应的化学方程式是______.
②装置E的试管中溶液变无色,取该溶液加热,溶液又变为红色,其原因是______.
③此装置有一个明显的不足之处是______.
④活性炭也能使品红溶液褪色,其褪色原理与二氧化硫使品红溶液褪色的原理不相同,其理由是______.
[反思提高]某同学将二氧化硫通入到紫色的酸性高锰酸钾溶液中,观察到溶液由紫色变为无色,由此他得出的结论是:二氧化硫能将酸性高锰酸钾溶液漂白.请你设计实验证明此结论是否正确(要求写出操作、现象、结论):______.
二氧化硫与二氧化碳有相似的化学性质,但二氧化硫还具有某些特殊的化学性质.
【答案】分析:(1)依据二氧化碳溶于水生成碳酸,二氧化碳与石灰水反应生成碳酸钙的知识分析解决;
(2)①根据二氧化硫能与石灰水反应生成白色的亚硫酸钙的知识解决;
②依据题干中有关二氧化硫的使溶液褪色的原理分析判断;
③依据二氧化硫是有毒气体,需进行尾气处理的知识分析判断;
④从两者使物质褪色的变化类型分析判断;
【反思提高】根据二氧化硫的漂白原理进行分析判断即可
解答:解:(1)二氧化碳溶于水生成碳酸,碳酸能使石蕊变红,二氧化碳与石灰水反应生成碳酸钙沉淀和水,所以溶液变浑浊;
(2)①结合题干中的叙述可知:二氧化硫能与石灰水反应生成白色的亚硫酸钙和水,其方程式为:SO2+Ca(OH)2═CaSO3↓+H2O;
②二氧化硫的使溶液褪色的原理是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,所以取该溶液加热,溶液又变为红色,其原因是 二氧化硫与品红溶液反应生成不稳定的无色物质,加热又分解生成了品红;
③二氧化硫是有毒气体,不能排放到空气中污染空气,所以该装置需进行尾气处理以防空气污染;
④两者使物质褪色的变化类型不同:活性炭的吸附溶液褪色的过程是物理变化,而二氧化硫使溶液褪色是化学变化;
【反思提高】二氧化硫的漂白原理是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,所以可进行如下设计:将褪色的溶液加热,观察溶液颜色的变化,若溶液恢复为原来的颜色,则结论正确,否则错误.
故答案为:(1)紫色石蕊变红,CO2+Ca(OH)2═CaCO3↓+H2O;
(2)①SO2+Ca(OH)2═CaSO3↓+H2O;
②二氧化硫与品红溶液反应生成不稳定的无色物质,加热又分解生成了品红;
③需进行尾气处理;
④活性炭的吸附过程是物理变化,而二氧化硫使溶液褪色是化学变化;
【反思提高】将褪色的溶液加热,观察溶液颜色的变化,若溶液恢复为原来的颜色,则结论正确,否则错误.
点评:此题是一道实验设计题,解题的关键是掌握二氧化碳的性质并进行知识的大胆迁移,只有这样才能顺利解题.
(2)①根据二氧化硫能与石灰水反应生成白色的亚硫酸钙的知识解决;
②依据题干中有关二氧化硫的使溶液褪色的原理分析判断;
③依据二氧化硫是有毒气体,需进行尾气处理的知识分析判断;
④从两者使物质褪色的变化类型分析判断;
【反思提高】根据二氧化硫的漂白原理进行分析判断即可
解答:解:(1)二氧化碳溶于水生成碳酸,碳酸能使石蕊变红,二氧化碳与石灰水反应生成碳酸钙沉淀和水,所以溶液变浑浊;
(2)①结合题干中的叙述可知:二氧化硫能与石灰水反应生成白色的亚硫酸钙和水,其方程式为:SO2+Ca(OH)2═CaSO3↓+H2O;
②二氧化硫的使溶液褪色的原理是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,所以取该溶液加热,溶液又变为红色,其原因是 二氧化硫与品红溶液反应生成不稳定的无色物质,加热又分解生成了品红;
③二氧化硫是有毒气体,不能排放到空气中污染空气,所以该装置需进行尾气处理以防空气污染;
④两者使物质褪色的变化类型不同:活性炭的吸附溶液褪色的过程是物理变化,而二氧化硫使溶液褪色是化学变化;
【反思提高】二氧化硫的漂白原理是二氧化硫与某些有色物质(如品红溶液)反应生成不稳定的无色物质,所以可进行如下设计:将褪色的溶液加热,观察溶液颜色的变化,若溶液恢复为原来的颜色,则结论正确,否则错误.
故答案为:(1)紫色石蕊变红,CO2+Ca(OH)2═CaCO3↓+H2O;
(2)①SO2+Ca(OH)2═CaSO3↓+H2O;
②二氧化硫与品红溶液反应生成不稳定的无色物质,加热又分解生成了品红;
③需进行尾气处理;
④活性炭的吸附过程是物理变化,而二氧化硫使溶液褪色是化学变化;
【反思提高】将褪色的溶液加热,观察溶液颜色的变化,若溶液恢复为原来的颜色,则结论正确,否则错误.
点评:此题是一道实验设计题,解题的关键是掌握二氧化碳的性质并进行知识的大胆迁移,只有这样才能顺利解题.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是 (填实验步骤序号).
(2)步骤、中研磨固体所用仪器的名称是 .
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
(3)上述实验中的“待测数据”指 .
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a. ;
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
Ⅰ.制取氧化铜
①称取2gCuSO4?5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是
(2)步骤、中研磨固体所用仪器的名称是
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL
 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g | 0.5g CuO | |
| ⑥ | 1.2g | 0.5g MnO2 |
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a.
b.检验CuO的化学性质是否改变.
c.查阅资料后了解,MnO2对KClO3的催化过程由以下三个反应组成,请将第二个反应补充完整.
a.KClO3+2MnO2=2KMnO4+Cl2+O2↑
b.2KMnO4→K2MnO4+
c.K2MnO4+Cl2=2KCl+MnO2+O2↑
某实验小组欲用10克胆矾制取氧化铜并证明氧化铜能加快H2O2的分解.
Ⅰ.请你完成他们制取氧化铜的实验步骤.
(1)称取10克胆矾,将其放入小烧杯中,再______.
(2)向步骤(1)中的烧杯内滴加______溶液,直至产生大量的沉淀.
(3)检验硫酸铜是否被作用完全,操作方法是______
______.
(4)将步骤(2)所得的混合物加热至沉淀全部变为黑色氧化铜.
(5)再将步骤(4)所得混合物过滤、洗涤、烘干后研细;验证是否洗净沉淀中硫酸根离子的方法是______
______.
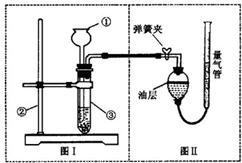
Ⅱ.小明设计了如图实验装置来证明氧化铜能加快双氧水(浓度约7%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:

(1)从设计装置来看,有一个明显的缺陷,你认为如何纠正______.
(2)从设计原理看,实验中的“待测数据”可以是指______.
(3)实验时气体收集在图Ⅱ的球型漏斗中.若要保证读取的气体体积没有误差,在读数前应进行的操作是______.若要检验产生的气体是氧气,应打开单孔橡皮塞,______.
(4)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验(不必写具体操作):a.证明CuO的化学性质没有改变;b.______.
Ⅲ.为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是______.
Ⅰ.请你完成他们制取氧化铜的实验步骤.
(1)称取10克胆矾,将其放入小烧杯中,再______.
(2)向步骤(1)中的烧杯内滴加______溶液,直至产生大量的沉淀.
(3)检验硫酸铜是否被作用完全,操作方法是______
______.
(4)将步骤(2)所得的混合物加热至沉淀全部变为黑色氧化铜.
(5)再将步骤(4)所得混合物过滤、洗涤、烘干后研细;验证是否洗净沉淀中硫酸根离子的方法是______
______.
Ⅱ.小明设计了如图实验装置来证明氧化铜能加快双氧水(浓度约7%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率).用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
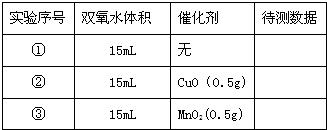
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| ① | 15mL | 无 | |
| ② | 15mL | CuO(0.5g) | |
| ③ | 15mL | MnO2(0.5g) |

(1)从设计装置来看,有一个明显的缺陷,你认为如何纠正______.
(2)从设计原理看,实验中的“待测数据”可以是指______.
(3)实验时气体收集在图Ⅱ的球型漏斗中.若要保证读取的气体体积没有误差,在读数前应进行的操作是______.若要检验产生的气体是氧气,应打开单孔橡皮塞,______.
(4)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验(不必写具体操作):a.证明CuO的化学性质没有改变;b.______.
Ⅲ.为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是______.