题目内容
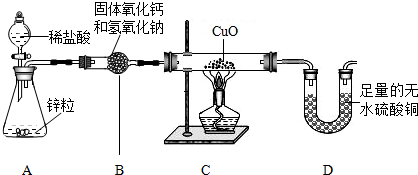
实验室用纯净、干燥的的氢气还原氧化铜来测定水中氢元素和氧元素的质量之比(本实验制得的氢气中可能混有氯化氢和水蒸气)。设计如下实验装置:

回答下列问题:
①实验开始时,应该先 ⑿ b(选填字母)。
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是 ⒀ 。
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是 ⒁ 。若要避免有氯化氢气体产生,装置A中试剂应改成 ⒂ 溶液。
③装置C中的实验现象是 ⒃ 。
④反应后其数据如下表所示:
| 反应前 | 反应后 | |
| (氧化铜+玻璃管)质量/g | 89.5 | 86.3 |
| (硫酸铜+U型管)质量/g | 214.4 | 218.0 |
根据实验数据填空,生成水中氢元素的质量为 ⒄ 克。
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会
⒅ (填“偏小”或“偏大”或“无影响”)。
| ⑿ | b | |
| ② | ⒀ | 除去氯化氢气体和水蒸气 答全给分 |
| ⒁ | 在AB之间添加盛有硝酸银溶液的装置 合理给分 | |
| ⒂ | 稀硫酸 | |
| ③ | ⒃ | 黑色固体变成亮红色 |
| ④ | ⒄ | 0.4 |
| ⑤ | ⒅ | 偏大 |

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
实验室用纯净、干燥的氢气还原氧化铜来测定水中氢元素和氧元素的质量之比(本实验制得的氢气中可能混有氯化氢和水蒸气).设计如下实验装置:

回答下列问题:
①实验开始时,应该先______(选填字母).
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是______.
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是______.若要避免有氯化氢气体产生,装置A中试剂应改成______溶液.
③装置C中的实验现象是______.
④反应后其数据如下表所示:
根据实验数据填空,生成水中氢元素的质量为______克.
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会______(填“偏小”或“偏大”或“无影响”).

回答下列问题:
①实验开始时,应该先______(选填字母).
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是______.
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是______.若要避免有氯化氢气体产生,装置A中试剂应改成______溶液.
③装置C中的实验现象是______.
④反应后其数据如下表所示:
| 反应前 | 反应后 | |
| (氧化铜+玻璃管)质量/g | 89.5 | 86.3 |
| (硫酸铜+U型管)质量/g | 214.4 | 218.0 |
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会______(填“偏小”或“偏大”或“无影响”).
实验室用纯净、干燥的氢气还原氧化铜来测定水中氢元素和氧元素的质量之比(本实验制得的氢气中可能混有氯化氢和水蒸气).设计如下实验装置:

回答下列问题:
①实验开始时,应该先______(选填字母).
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是______.
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是______.若要避免有氯化氢气体产生,装置A中试剂应改成______溶液.
③装置C中的实验现象是______.
④反应后其数据如下表所示:
根据实验数据填空,生成水中氢元素的质量为______克.
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会______(填“偏小”或“偏大”或“无影响”).

回答下列问题:
①实验开始时,应该先______(选填字母).
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是______.
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是______.若要避免有氯化氢气体产生,装置A中试剂应改成______溶液.
③装置C中的实验现象是______.
④反应后其数据如下表所示:
| 反应前 | 反应后 | |
| (氧化铜+玻璃管)质量/g | 89.5 | 86.3 |
| (硫酸铜+U型管)质量/g | 214.4 | 218.0 |
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会______(填“偏小”或“偏大”或“无影响”).
实验室用纯净、干燥的氢气还原氧化铜来测定水中氢元素和氧元素的质量之比(本实验制得的氢气中可能混有氯化氢和水蒸气).设计如下实验装置:

回答下列问题:
①实验开始时,应该先______(选填字母).
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是______.
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是______.若要避免有氯化氢气体产生,装置A中试剂应改成______溶液.
③装置C中的实验现象是______.
④反应后其数据如下表所示:
根据实验数据填空,生成水中氢元素的质量为______克.
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会______(填“偏小”或“偏大”或“无影响”).

回答下列问题:
①实验开始时,应该先______(选填字母).
a.给氧化铜加热 b.打开分液漏斗的活塞滴加酸液
②装置B的作用是______.
实验中若要验证氢气中混有氯化氢,该实验中改进的方法是______.若要避免有氯化氢气体产生,装置A中试剂应改成______溶液.
③装置C中的实验现象是______.
④反应后其数据如下表所示:
| 反应前 | 反应后 | |
| (氧化铜+玻璃管)质量/g | 89.5 | 86.3 |
| (硫酸铜+U型管)质量/g | 214.4 | 218.0 |
⑤上图中若没有装置B,并且不考虑空气中水分的影响,则测定结果中氢元素的质量会______(填“偏小”或“偏大”或“无影响”).