题目内容
金属及金属材料在生产、生活中应用广泛。
(1)铜可以拉成铜丝,这是利用金属的_________。
(2)铝具有很好的抗腐蚀性能,原因是____________________(用化学方程式表示)。
(3)小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):

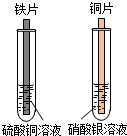
①将铁片插入硫酸铜溶液中,铁片表面的现象是_____________________;
②将铜片插入硝酸银溶液中,反应的化学方程式是__________________。
此探究实验的目的是________________________________。
【解析】(1)铜可以拉成铜丝是将铜进行延长,利用铜具有优良的延展性。
(2)铝有很好的抗腐蚀性是因为铝会与空气中的氧气反应,在表面形成一支致密的氧化膜(成分为氧化铝),从而使里面的铝不会被腐蚀。反应的化学方程式为:4Al+3O2=2Al2O3
(3)①将铁片插入硫酸铜溶液中:因为铁的活动性比铜强,所以铁会将铜从其盐溶液中置换出来,因此在铁的表面会出现紫红物的物质(铜)。
②将铜片插入硝酸银溶液中:因为铜的活动性比银强,所以铜会将银从其盐溶液中置换出来。反应为:Cu+2AgNO3=Cu(NO3)2+2Ag
通过上述两个实验可以确定铁铜银三种金属的活动性顺序。(答成结论如:活动性顺序为铁>铜>银 是该实验的结论而不是实验的目的,不符合题意)

练习册系列答案
相关题目

 (2013?咸宁)如图,金属及金属材料在生产、生活中应用广泛.
(2013?咸宁)如图,金属及金属材料在生产、生活中应用广泛. 如图,金属及金属材料在生产、生活中应用广泛.
如图,金属及金属材料在生产、生活中应用广泛. 如图,金属及金属材料在生产、生活中应用广泛.
如图,金属及金属材料在生产、生活中应用广泛.