题目内容
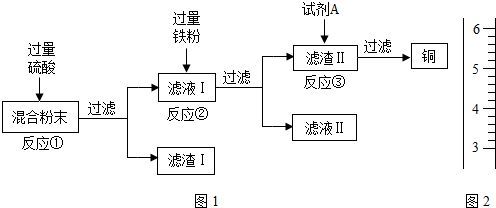
木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案(图1)如下:

(1)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需______g98%的硫酸和______g水.实际操作时,用lOmL量筒取98%的硫酸(密度为1.84g/cm3),请在答题卡图2中画出所取硫酸的液面.
(2)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入______中(填仪器名称),然后______ (填操作名称),使反应充分进行.
(3)试剂A可选用______溶液(填一种物质的化学式).
(4)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)______.
解:(1)需要98%的硫酸的质量为 =10g;需要水的质量为40g-10g=30g,需要浓硫酸的体积为:
=10g;需要水的质量为40g-10g=30g,需要浓硫酸的体积为: =5.4mL;
=5.4mL;
(2)较多量试剂的反应容器可在烧杯中,为了加快反应速率可用玻璃棒不断搅拌;
(3)滤渣Ⅱ中含有剩余的铁粉,因此可加入硫酸或硫酸铜除去;
(4)开始混合粉末中的铜没有和酸反应,进入滤渣Ⅰ中,为了回收更多的铜,可将滤渣Ⅰ中的铜也回收,或将滤渣I在空气中充分灼烧,再投入反应①中;
故答案为:
(1)10g;30g; 所取硫酸的体积为5.4mL(如右图所示)
(2)烧杯;用玻璃棒不断搅拌;
(3)H2SO4(合理均可);
(4)回收滤渣I中的Cu(或将滤渣I在空气中充分灼烧,再投入反应①中).
分析:(1)根据溶质质量分数的计算公式及公式变形分析求解,并据量筒正确读法分析解答;
(2)烧杯可用作较多试剂进行反应的容器,为使反应充分进行,可用玻璃棒搅拌;
(3)要除去铜粉中的铁粉,可加入稀硫酸;
(4)要得到更多的铜,可将反应过程中的铜回收或再利用.
点评:解答时关健是看明白流程图中各物质的转化关系,发生的化学反应,过量物质的去向,以及如何依据物质的性质除去过量物质.
 =10g;需要水的质量为40g-10g=30g,需要浓硫酸的体积为:
=10g;需要水的质量为40g-10g=30g,需要浓硫酸的体积为: =5.4mL;
=5.4mL;(2)较多量试剂的反应容器可在烧杯中,为了加快反应速率可用玻璃棒不断搅拌;
(3)滤渣Ⅱ中含有剩余的铁粉,因此可加入硫酸或硫酸铜除去;
(4)开始混合粉末中的铜没有和酸反应,进入滤渣Ⅰ中,为了回收更多的铜,可将滤渣Ⅰ中的铜也回收,或将滤渣I在空气中充分灼烧,再投入反应①中;
故答案为:
(1)10g;30g; 所取硫酸的体积为5.4mL(如右图所示)

(2)烧杯;用玻璃棒不断搅拌;
(3)H2SO4(合理均可);
(4)回收滤渣I中的Cu(或将滤渣I在空气中充分灼烧,再投入反应①中).
分析:(1)根据溶质质量分数的计算公式及公式变形分析求解,并据量筒正确读法分析解答;
(2)烧杯可用作较多试剂进行反应的容器,为使反应充分进行,可用玻璃棒搅拌;
(3)要除去铜粉中的铁粉,可加入稀硫酸;
(4)要得到更多的铜,可将反应过程中的铜回收或再利用.
点评:解答时关健是看明白流程图中各物质的转化关系,发生的化学反应,过量物质的去向,以及如何依据物质的性质除去过量物质.

练习册系列答案
相关题目
(13分)木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下:
(1)写出下列反应的化学方程式:
反应①:______________________; 反应②:___________________________.
(2)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需________g 98%的硫酸和_______g水.
(3)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入__________中(填仪器名称),然后__________ (填操作名称),使反应充分进行.
(4)试剂A可选用___________溶液(填一种物质的化学式)
(5)已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜 想】猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有 (填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的_______,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有 . |
| ②取步骤①所得滤渣,加过量的_________,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有 . |
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式 .