题目内容
盐酸与氢氧化钠溶液发生反应过程中溶液的pH变化如图一,请分析并回答问题:

(1)由图一可判断,该反应的实验过程是按照图二中的 (填“图甲”或“图乙”)来进行的.
(2)图一中A、B、C三点表示的溶液,两种反应物恰好完全反应的点是 点,加入紫色石蕊试液会呈现红色的是 点的溶液,此时溶液中的含有的阳离子是 .

(1)由图一可判断,该反应的实验过程是按照图二中的
(2)图一中A、B、C三点表示的溶液,两种反应物恰好完全反应的点是
考点:中和反应及其应用,酸碱指示剂及其性质,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:根据图一可知,点A处表示溶液显酸性、点C处溶液显中性、点B处溶液显碱性.根据曲线变化趋势可以判定,该反应中是氢氧化钠过量.
解答:解:(1)由图示看出,溶液的pH是由小于7到等于7再到大于7,是由酸性到中性再到碱性,甲图是向碱溶液中滴加酸,乙图是向酸中滴加碱溶液,符合图一pH变化的应该是向碱溶液中加酸;
(2)盐酸和氢氧化钠完全中和时,溶液呈中性,pH=7,则是C点;酸性溶液能使紫色石蕊试液变红色,酸性溶液的pH小于7,酸性溶液中有氯化钠和HCl.
故答案是:(1)图甲 (2)C;A;氢离子和钠离子.
(2)盐酸和氢氧化钠完全中和时,溶液呈中性,pH=7,则是C点;酸性溶液能使紫色石蕊试液变红色,酸性溶液的pH小于7,酸性溶液中有氯化钠和HCl.
故答案是:(1)图甲 (2)C;A;氢离子和钠离子.
点评:本题是考查中和反应过程中溶液pH的变化情况的,我们要知道向酸中加碱和向碱中加酸时,溶液pH的变化趋向.明确不同指示剂的变色范围.

练习册系列答案
相关题目
某无色混合气体可能含有水蒸气、二氧化碳、一氧化碳、氯化氢和氢气.当混合气体通过浓硫酸后气体体积没有变化;再通过澄清石灰水,也没有出现明显变化,但是气体体积减少一半;点燃导出的气体,将燃烧产物通过无水硫酸铜不变色,却能使澄清石灰水变浑浊.则下列关于混合气体的说法不正确的是( )(注:无水硫酸铜遇水变蓝色)
| A、混合气体中肯定没有氢气、水蒸气 |
| B、混合气体中一定有氯化氢 |
| C、混合气体中可能有二氧化碳 |
| D、混合气体中可能有一氧化碳 |

 第45届世界体操锦标赛将于2014年10月3日至12日在广西体育中心体育馆举行.
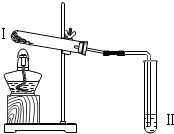
第45届世界体操锦标赛将于2014年10月3日至12日在广西体育中心体育馆举行. 点燃不纯的可燃性气体可能发生爆炸,如图是某同学的改进装置.请回答.
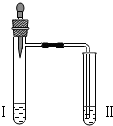
点燃不纯的可燃性气体可能发生爆炸,如图是某同学的改进装置.请回答. 如图是某研究性学习小组进行CO2与NaOH溶液反应的探究实验装置.
如图是某研究性学习小组进行CO2与NaOH溶液反应的探究实验装置.