题目内容
焊锡是锡铅合金,把铅加入锡中制成合金的主要目的是( )
A.增加强度 B.降低熔点
C.增加延展性 D.增强 抗腐蚀性
抗腐蚀性
选B。焊锡是焊接用的一种金属材料,要求熔点要低,故选B。

 名校课堂系列答案
名校课堂系列答案生铁和钢都是铁的合金。下表对生铁和钢的成分、性能作了比较。
| 生铁 | 钢 | |
| 含碳量 | 2%~4.3% | 0. |
| 性能 | 硬而脆、无韧性、可铸、不可煅轧 | 坚硬而有韧性、可铸、可煅轧 |
根据表中提供的信息,回答下列问题:
(1)与生铁相比,钢有什么优良的性能?(答出一条即可)
。
(2)写出钢的一条用途:
 。
。
(3)比较生铁与钢的成分,说明生铁与钢在性能上有较大差异的主要原因:
。
高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
(1)试管尾部放一团湿棉花的目的是 。
(2)探究生成的气体是什么? 用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是______________。写出该反应的化学方程 式 。
式 。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 与盐酸反应 | FeCl2+H2O | FeCl3+H2O | FeCl2+ FeCl3+H2O |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是 ;猜想二:剩余固体________。
【实验探究】(每空2分)
| 实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为_______________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
(4)若反应前称得铁的质量为2.1g,高温下,铁与水反应结束称得固体质量为2.8 g则剩余固体成分是 。(通过计算说明,要求写出计算过程)
g则剩余固体成分是 。(通过计算说明,要求写出计算过程)
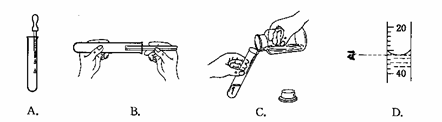
 金属单元后,小强知道了铁是当今世界用量最多的金属,而每年全世界被腐蚀损耗的钢铁材料,约占全年钢铁产量的十分之一。于是小强对金属铁的相关知识开展了探究性学习。
金属单元后,小强知道了铁是当今世界用量最多的金属,而每年全世界被腐蚀损耗的钢铁材料,约占全年钢铁产量的十分之一。于是小强对金属铁的相关知识开展了探究性学习。 、B、C三处的变化。几天后,他发现 (填序号)处最先出现铁锈,小强结合书本知识知道,铁生锈实际是铁和 、 等物质发生反应的过程。
、B、C三处的变化。几天后,他发现 (填序号)处最先出现铁锈,小强结合书本知识知道,铁生锈实际是铁和 、 等物质发生反应的过程。
 03%~2%
03%~2%
 中除了含有CO2,还可能含有少量__________。实验室常用__________的方法检验这种可能含有的气体。
中除了含有CO2,还可能含有少量__________。实验室常用__________的方法检验这种可能含有的气体。