题目内容
实验室用6.5 g锌与足量稀硫酸反应,可制得氢气的质量是多少?
解:制得氢气的质量为x
Zn+H2SO4 == ZnSO4 +H2 ↑
65 2
6.5 g x


答:制得氢气的质量为0.2 g。
Zn+H2SO4 == ZnSO4 +H2 ↑
65 2
6.5 g x


答:制得氢气的质量为0.2 g。

练习册系列答案
相关题目
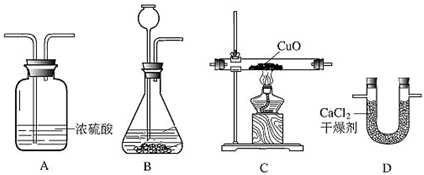
某化学兴趣小组的同学利用下列装置进行实验室制取气体的探究.请你参与探究并回答下列问题.

(1)完成下表:
如图:
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是 原因是: .
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是 (填写选项序号).
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当 停止加热.
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为 .请在装有所配制溶液的试剂瓶(如图)标签上标明相应信息.
④过滤、溶解、蒸发时都需用到的仪器是 (填序号);
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是 .

(1)完成下表:
| 气 体 | 药 品 | 装置组合 | 反应的化学方程式 |
| 氧 气 | 氯酸钾和二氧化锰 | ||
| 氢 气 | 稀盐酸与锌粒 | A、C | |
| 二氧化碳(干燥) | 大理石和稀盐酸 |
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为

④过滤、溶解、蒸发时都需用到的仪器是
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是
某化学兴趣小组的同学利用下列装置进行实验室制取气体的探究.请你参与探究并回答下列问题.

(1)完成下表:
如图:
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是 原因是: .
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是 (填写选项序号).
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当 停止加热.
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为 .请在装有所配制溶液的试剂瓶(如图)标签上标明相应信息.
④过滤、溶解、蒸发时都需用到的仪器是 (填序号);
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是 .


(1)完成下表:
| 气 体 | 药 品 | 装置组合 | 反应的化学方程式 |
| 氧 气 | 氯酸钾和二氧化锰 | ||
| 氢 气 | 稀盐酸与锌粒 | A、C | |
| 二氧化碳(干燥) | 大理石和稀盐酸 |
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是 原因是: .
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是 (填写选项序号).
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当 停止加热.
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为 .请在装有所配制溶液的试剂瓶(如图)标签上标明相应信息.
④过滤、溶解、蒸发时都需用到的仪器是 (填序号);
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是 .