题目内容
100g某硫酸钠溶液恰好跟100g溶质质量分数为17.1%的氢氧化钡溶液完全反应[化学方程式为Na2S04+Ba(OH)2═BaS04↓+2NaOH].
求:
(1)生成硫酸钡的质量.
(2)反应所得溶液的溶质质量分数.
求:
(1)生成硫酸钡的质量.
(2)反应所得溶液的溶质质量分数.
分析:根据反应的化学方程式进行计算,求出生成的硫酸钡的质量,然后根据溶质质量分数公式求出溶液的溶质质量分数.
解答:解:设生成硫酸钡的质量为x生成氢氧化钠的质量为y
Na2S04+Ba(OH)2═BaS04↓+2NaOH
171 233 80
100g×17.1% x y
=
=
x=23.3g
y=8g
(2)反应所得溶液的溶质质量分数为:
×100%=4.5%
答;(1)生成硫酸钡的质量23.3g.
(2)反应所得溶液的溶质质量分数为4.5%.
Na2S04+Ba(OH)2═BaS04↓+2NaOH
171 233 80
100g×17.1% x y
| 171 |
| 100g×17.1% |
| 233 |
| x |
| 80 |
| y |
x=23.3g
y=8g
(2)反应所得溶液的溶质质量分数为:
| 8g |
| 100g+100g-23.3g |
答;(1)生成硫酸钡的质量23.3g.
(2)反应所得溶液的溶质质量分数为4.5%.
点评:本题考查了根据化学方程式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
(1)根据所提供的溶解度数据,画出硫酸钠的溶解度曲线.
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是 g,溶质的质量分数是 (精确到0.1%).
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下: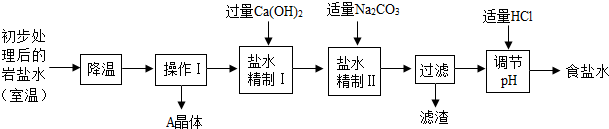
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是 .
(4)“操作I”中的操作是 ,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有 .
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是 .
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是 .
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:

(3)“降温”的目的是析出副产品“A晶体”,A的化学式是
(4)“操作I”中的操作是
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是

 ′
′