题目内容
20.(1)锂是一种金属单质,化学式为 Li,锂原子结构示意图为 ,易失去最外层一个电子.则锂的氧化物的化学式为Li2O,氢氧化锂是一种极易溶于水的白色固体有强碱性,载人航天飞船中通常用氢氧化锂来吸收航天员产生的二氧化碳,生成碳酸锂和水,则氢氧化锂与二氧化碳反应的化学方程式为CO2+2LiOH=Li2CO3+H2O
,易失去最外层一个电子.则锂的氧化物的化学式为Li2O,氢氧化锂是一种极易溶于水的白色固体有强碱性,载人航天飞船中通常用氢氧化锂来吸收航天员产生的二氧化碳,生成碳酸锂和水,则氢氧化锂与二氧化碳反应的化学方程式为CO2+2LiOH=Li2CO3+H2O(2)化学反应 A→B+C,D 在反应中作催化剂,12gA 和3gD 混合后使反应完全,生成了8gB,问同时生成4gC.
分析 (1)根据原子结构示意图的画法,画出原子结构示意图,根据原子的最外层的电子数主要决定了元素的性质,分析写出锂的氧化物的化学式;根据化学方程式的写法写出化学方程式.
(2)根据质量守恒定律,反应前参加反应的物质的质量总和与反应后生成的各物质质量和相等,催化剂在反应前后质量不变,可判断该反应中生成物质B与C的质量和与物质A的质量相等.
解答 解:(1)锂的质子数是3,核外电子数是3,第一层最多排两个电子,所以第二层排一个电子,所以锂原子结构示意图为 ,由锂的结构示意图可知,在形成化合物时,锂易失去最外层一个电子,故化合价表现为+1价,而氧元素为-2价,故锂的氧化物的化学式为Li2O;因二氧化碳与氢氧化锂反应生成碳酸锂和水,用观察法配平即可,所以方程式是:CO2+2LiOH=Li2CO3+H2O;
,由锂的结构示意图可知,在形成化合物时,锂易失去最外层一个电子,故化合价表现为+1价,而氧元素为-2价,故锂的氧化物的化学式为Li2O;因二氧化碳与氢氧化锂反应生成碳酸锂和水,用观察法配平即可,所以方程式是:CO2+2LiOH=Li2CO3+H2O;
(2)由质量守恒定律可知,生成C物质的质量=12g-8g=4g;
故答案为:(1) ;Li2O;CO2+2LiOH=Li2CO3+H2O;(2)4.
;Li2O;CO2+2LiOH=Li2CO3+H2O;(2)4.
点评 本题主要考查了原子的结构及质量守恒定律的知识.利用质量守恒定律,由反应前后物质质量总和相等,可计算反应中某物质的质量.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
12.如图是利用缺铁性氧化物[Fe(1-y)O]进行CO2再资源化研究的示意图.下列说法不正确的是( )

| A. | 如该研究成熟并广泛应用,能缓解温室效应 | |
| B. | 反应②为化合反应 | |
| C. | 反应①提高了铁的氧化物中铁的质量分数 | |
| D. | 整个转化反应的化学方程式可表示为:CO2$\frac{\underline{\;高温\;}}{\;}$C+O2 |
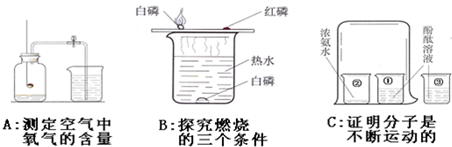
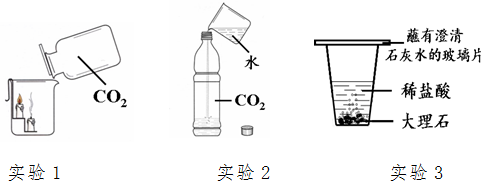


 如图为研究冶炼铁的化学原理的装置,指出A、B处出现的现象,并写出化学反应方程式:
如图为研究冶炼铁的化学原理的装置,指出A、B处出现的现象,并写出化学反应方程式: