题目内容
如右图所示,某无色溶液能分别与四种物质发生反应,则下列说法正确的是( )
A.溶液X一定是稀盐酸
B.黄色溶液中的溶质为FeCl2
C.溶液X能使无色酚酞试剂变红
D.X与铁反应后,生成浅绿色溶液和氢气
B、根据铁离子在溶液中显黄色进行分析;
C、根据酸不会使酚酞变色进行分析;
D、根据亚铁离子在溶液中显浅绿色进行分析.
解答:解:A、无色溶液X时石蕊变红色,说明X显酸性,X和碳酸钠反应生成气体,说明X中存在氢离子,但是不能说明就是盐酸,硫酸也可以,故A错误;
B、铁离子在溶液中显黄色,氧化铁和酸会生成三价的铁盐,故B错误;
C、无色溶液X时石蕊变红色,说明X显酸性,X和碳酸钠反应生成气体,说明X中存在氢离子,酚酞遇酸性液体不变色,故C错误;
D、无色溶液X时石蕊变红色,说明X显酸性,X和碳酸钠反应生成气体,说明X中存在氢离子,氢离子和铁反应会生成亚铁离子和氢气,故D正确;
故选D.
点评:在解此类题时,首先通过体中的反应现象确定需要鉴别的物质的性质,然后对照选项进行分析解答.

 星级口算天天练系列答案
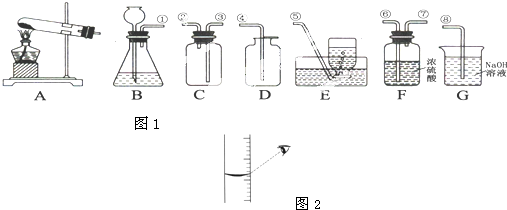
星级口算天天练系列答案某化学兴趣小组的同学对 “硫酸、硝酸钡、氢氧化钠、碳酸钠”四种物质之间的反应进行了定性和定量的研究。根据复分解反应发生的条件,初步判断上述四种溶液两两之间能发生 个反应;其中有气体、沉淀生成的化学方程式为:(请各写出一个)
(1) ;(2) 。
【实验一】证明氢氧化钠溶液和稀硫酸混合后确实发生了化学反应
王同学按下列方法进行了实验:

请回答:
在A的实验中,滴入紫色石蕊溶液的目的是 ;
B装置中发生的化学反应方程式为 ;
|
【实验二】定量分析稀硫酸与两种混合物反应后溶液的成分
刘同学称取38.2g氢氧化钠和碳酸钠的混合溶液于烧杯中,
向其中逐滴滴加质量分数为15.3%的稀硫酸,同时记录实验数据,
测得加入稀硫酸的质量与生成气体的质量关系如右图所示。
①当加入16g稀硫酸时,溶液中的溶质
为 (写化学式)
②求混合物与稀硫酸恰好完全反应时所得
溶液的溶质质量分数。(请写出计算过程,结果保留到0.1%)
【实验三】实验分析四种化合物溶液混合后的成分
洪同学按以下流程进行了实验:

操作Ⅰ的名称是 ,固体D的化学式是 ;
如溶液B中滴入酚酞,呈无色,则B中一定没有 离子;一定含有 离子。
【解析】根据物质的性质进行分析,物质间混合时若能生成沉淀、气体或水,则反应能够进行,氢氧化钠与稀硫酸反应生成硫酸钠和水,没有明显的实验现象,可以通过指示剂进行指示,在氢氧化钠和碳酸钠的混合液中加入硫酸,硫酸先与氢氧化钠反应,再与碳酸钠反应,根据图象提供的数据进行计算,分离不溶性固体和可溶性固体使用过滤的方法,酚酞在碱性溶液中为红色,在中性和酸性溶液中为无色.
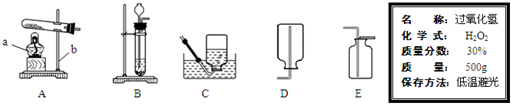
 23、某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究.请你参与他们的探究活动,并回答有关问题.
23、某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究.请你参与他们的探究活动,并回答有关问题.