题目内容
4. 某化学兴趣小组进行溶液的配制和粗盐的初步提纯实验.
某化学兴趣小组进行溶液的配制和粗盐的初步提纯实验. (1)配制150克质量分数为10%的氢氧化钠为溶液,
①计算:需要氢氧化钠固体的质量为15克,需要水的体积为135mL(水的密度近似看作1g/mL
②称量:调节托盘天平平衡后,将烧杯放在托盘天平的左盘,称量其质量,然后 在右盘添加砝码,最后添加氢氧化钠固体,至到天平平衡.
③用量筒量取所需要的水,倒入盛有氢氧化钠固体的烧杯中,用玻璃棒搅拌,使其溶解,并冷却到室温.
④存贮:将配制好的溶液放入试剂瓶,塞好橡胶塞并贴上标签,放到指定的地方.
(2)粗盐的初步提纯:①称取5.0克粗盐,用药匙逐渐加入到10mL水中,直到粗盐不再溶解为止.还需进行的实验操作步骤的顺序为:称量剩余粗盐、A、C、D、B(填编号)
A 过滤 B 计算产率 C 蒸发 D称量精盐
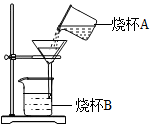
②过滤操作如图所示,指出其中的错误之处:未用玻璃棒引流;滤纸边缘高出漏斗边缘;漏斗下端尖嘴未紧靠烧杯B的内壁.
分析 (1)溶质质量=溶液质量×溶质质量分数;
氢氧化钠固体易潮解,应该放在玻璃器皿中称量;
(2)还需进行的实验操作步骤的顺序为:称量剩余粗盐、过滤、蒸发、称量精盐质量、计算产率;
②过滤时,应该用玻璃棒引流,滤纸边缘应该低于漏斗边缘,漏斗尖嘴应该紧贴烧杯内壁.
解答 解:(1)①需要氢氧化钠固体的质量为:150g×10%=15g,需要水的体积为:(150g-15g)÷1g/mL=135mL.
故填:15;135.
②称量:调节托盘天平平衡后,将烧杯放在托盘天平的左盘,称量其质量,然后在右盘添加砝码,最后添加氢氧化钠固体,至到天平平衡.
故填:烧杯;砝码.
③用量筒量取所需要的水,倒入盛有氢氧化钠固体的烧杯中,用玻璃棒搅拌,使其溶解,并冷却到室温.
故填:搅拌.
④将配制好的溶液放入试剂瓶,塞好橡胶塞并贴上标签,放到指定的地方.
故填:贴上标签.
(2)还需进行的实验操作步骤的顺序为:称量剩余粗盐、过滤、蒸发、称量精盐质量、计算产率.
故填:A、C、D、B.
②过滤时,应该用玻璃棒引流,滤纸边缘应该低于漏斗边缘,漏斗尖嘴应该紧贴烧杯内壁,因此其中的错误之处有:未用玻璃棒引流,滤纸边缘高出漏斗边缘,漏斗下端尖嘴未紧靠烧杯B的内壁.
故填:未用玻璃棒引流;滤纸边缘高出漏斗边缘;漏斗下端尖嘴未紧靠烧杯B的内壁.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
17.下列除去杂质(在括号内)选用的试剂(在箭头右侧)错误的是( )
| A. | CO2气体(H2O)→生石灰 | B. | C粉(CuO)→稀盐酸 | ||
| C. | CaCl2溶液(HC1)→碳酸钙粉末 | D. | Na2SO4溶液(CuSO4)→氢氧化钠溶液 |
9.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如下表所示).他从瓶中倒出50毫升用于配制成稀硫酸,(1毫升=1厘米3)请提取有用信息,求:
(1)这50毫升浓硫酸的质量为多少克?
(2)50毫升浓硫酸中纯硫酸质量是多少克?
(3)他将这50毫升浓硫酸与108g水均匀混合,所得稀硫酸的质量分数是多少?
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 |
(2)50毫升浓硫酸中纯硫酸质量是多少克?
(3)他将这50毫升浓硫酸与108g水均匀混合,所得稀硫酸的质量分数是多少?
16.对滤渣丙的分析正确的是( )
| A. | 若滤渣丙中有黑色固体,则滤渣丙中一定有铁 | |
| B. | 若滤液Ⅳ呈蓝色,则滤渣丙中一定有铁 | |
| C. | 若滤渣丙与固体丁的质量比大于4:5,则原固体由四种物质组成 | |
| D. | 若滤渣丙的质量小于固体丁的质量,则原固体由三种物质组成 |
13.下列离子符号书写正确的是( )
| A. | 铝离子 Al2+ | B. | 镁离子Mg2+ | C. | 碳酸根离子SO32- | D. | 钾离子 K1+ |