题目内容
【题目】钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇(CH4O)厂组成产业链可以大大提高资源利用率,减少环境污染。

请回答下列问题:
(1)电解食盐水生成烧碱、氯气、氢气的化学方程式为_____。
(2)钛铁矿被氯化后,除得到四氯化钛,还能制得用途广泛的化工产品X,该反应为2FeTiO3 + 6C + 7Cl2 ![]() 2X + 2TiCl4 + 6CO。则X的化学式为_____。
2X + 2TiCl4 + 6CO。则X的化学式为_____。
(3)由四氯化钛和镁通过置换反应制取钛的化学方程式为______,该过程中,氩气(Ar)的作用是_____。
(4)由CO和H2合成甲醇。若不考虑生产过程中物质的任何损失,上述产业链中每合成32吨甲醇,至少需H2的质量为___。
【答案】2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ FeCl3 2Mg+TiCl4
2NaOH+H2↑+Cl2↑ FeCl3 2Mg+TiCl4![]() 2MgCl2+Ti 隔绝空气,防止镁与空气中的成分(O2、CO2)反应 4t
2MgCl2+Ti 隔绝空气,防止镁与空气中的成分(O2、CO2)反应 4t
【解析】
本题是制取钛并把有毒的一氧化碳充分利用的流程题。
(1)电解食盐水生成烧碱、氯气、氢气的化学方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(2)根据反应2FeTiO3 + 6C + 7Cl2 ![]() 2X + 2TiCl4 + 6CO的微观含义推算X的化学式,反应前后Ti、O、C的原子个数相等,X一定不含Ti、O、C元素,反应前Fe原子个数为2个,则反应后2X中含铁原子也为2个,反应前氯原子个数为14个,反应后氯原子个数少了6个,则2X中含氯原子有6个,所以X一定含有铁元素和氯元素,且原子个数比为1:3,化学式为FeCl3。
2X + 2TiCl4 + 6CO的微观含义推算X的化学式,反应前后Ti、O、C的原子个数相等,X一定不含Ti、O、C元素,反应前Fe原子个数为2个,则反应后2X中含铁原子也为2个,反应前氯原子个数为14个,反应后氯原子个数少了6个,则2X中含氯原子有6个,所以X一定含有铁元素和氯元素,且原子个数比为1:3,化学式为FeCl3。
(3)由四氯化钛和镁通过置换反应制取钛的化学方程式为2Mg+TiCl4![]() 2MgCl2+Ti,该过程中,氩气(Ar)的作用是隔绝空气,防止镁与空气中的成分(O2、CO2)反应。
2MgCl2+Ti,该过程中,氩气(Ar)的作用是隔绝空气,防止镁与空气中的成分(O2、CO2)反应。
(4)解:设需H2的质量为X。

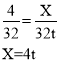
答:需H2的质量为4t。