题目内容
某同学为了测定实验室中氯酸钾样品的纯度.取2.5g该样品与0.5g二氧化锰混合,加热该混合物(杂质不参加反应),分别记录不同时刻剩余固体质量如下:
(1)加热t3时间后,该同学认为氯酸钾已经完全反应.理由 .
(2)根据质量守恒定律,该同学很快得到氧气的质量 克.
(3)求该样品中氯酸钾的纯度?
| 加热时间/min | t1 | t2 | t3 | t4 |
| 剩余固体/g | 2.12 | 2.08 | 2.04 | 2.04 |
(2)根据质量守恒定律,该同学很快得到氧气的质量
(3)求该样品中氯酸钾的纯度?
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据质量守恒定律固体物质的总质量的变化就可以求出生成的气体的质量,然后根据生成的氧气的质量,根据化学方程式进行计算就可求出参与反应的氯酸钾的质量.
解答:解:
(1)由于加热t3时间后,再继续加热时固体的质量没再发生变化,说明氯酸钾已经全部参与反应;
(2)氧气的质量为:2.5g+0.5g-2.04g=0.96g
(3)设样品中含有氯酸钾的质量为x
2KClO3
2KCl+3O2↑
245 96
x 0.96g
=
x=2.45g
样品中氯酸钾的质量分数为
×100%=98%
答:
(1)由于加热t3时间后,再继续加热时固体的质量没再发生变化,说明氯酸钾已经全部参与反应
(2)0.96
(3)样品中氯酸钾的质量分数为98%.
(1)由于加热t3时间后,再继续加热时固体的质量没再发生变化,说明氯酸钾已经全部参与反应;
(2)氧气的质量为:2.5g+0.5g-2.04g=0.96g
(3)设样品中含有氯酸钾的质量为x
2KClO3
| ||
| △ |
245 96
x 0.96g
| 245 |
| x |
| 96 |
| 0.96g |
x=2.45g
样品中氯酸钾的质量分数为
| 2.45g |
| 25g |
答:
(1)由于加热t3时间后,再继续加热时固体的质量没再发生变化,说明氯酸钾已经全部参与反应
(2)0.96
(3)样品中氯酸钾的质量分数为98%.
点评:本题难度不是很大,主要考查了根据化学方程式进行相关的计算及质量守恒定律的应用,培养学生的应用知识的能力和解决问题的能力.

练习册系列答案
相关题目
下列实验操作正确的是( )
A、 |
B、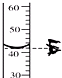 |
C、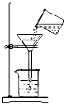 |
D、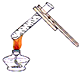 |
下列有关实验操作正确的是( )
| A、称量氢氧化钠固体时,将氢氧化钠固体直接放在纸上进行称量 |
| B、给蒸发皿加热时必须先垫石棉网 |
| C、用10mL量筒量取7.5mL的蒸馏水 |
| D、实验室制备蒸馏水的装置中,温度计必须插入液面以下 |
每年的6月26日是国际禁毒日,一种新型毒品K粉的主要成分是盐酸氯胺酮,盐酸氯胺酮的化学式为C13H16ONCl,它会对大脑造成永久损害.下列叙述中正确的是( )
| A、K粉是纯净物 |
| B、盐酸氯胺酮是氧化物 |
| C、盐酸氯胺酮由五个元素组成 |
| D、盐酸氯胺酮中氢元素和氧元素的质量分数相同 |
实验室制取二氧化碳有以下几个步骤:①按要求装好仪器 ②向漏斗中注入盐酸 ③向反应器中放入块状石灰石 ④检验装置气密性 ⑤收集生成气体 以上操作正确的排列顺序是( )
| A、①③②④⑤ |
| B、②①④③⑤ |
| C、①④③②⑤ |
| D、①②④③⑤ |
下列关于水的说法中,正确的是( )
| A、自来水是无色透明的,它是纯净物 |
| B、长期饮用纯净水,有益于人体健康 |
| C、我们应该节约用水,同时要防止水源受到污染 |
| D、矿泉水中含钾、钠、钙等多种物质,是一种健康饮料 |
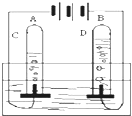 根据电解水实验装置图回答下列问题:
根据电解水实验装置图回答下列问题: