题目内容
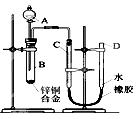
某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数。
⑴实验前,先将锌铜合金在稀酸中浸泡片刻,其目的是:____________________;
 ⑵实验操作步骤有:
⑵实验操作步骤有: 检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述再进行的操作的顺序是______________(填序号);记录C的液面位置时,除视线平视外,还应______________;
检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述再进行的操作的顺序是______________(填序号);记录C的液面位置时,除视线平视外,还应______________;
⑶B中发生反应的化学方程式为________________________ ____;
____;
⑷若实验用锌铜合金的质量为a g,与酸充分反应后,测得氢气体积为V L,为求出合金中锌、铜的质量分数,还缺少的一个数据是______________;
A.反应前加入稀酸的体积 B.反应前加入稀酸的质量分数
C.实验前反应装置中空气的体积 D.实验条件下氢气的密度
⑸若实验用锌铜合金 的质量为a g,与酸充分反应后,B中剩余固体的质量为b g,则锌的质量分数为______________;
的质量为a g,与酸充分反应后,B中剩余固体的质量为b g,则锌的质量分数为______________;
⑹实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将______________(填“偏大”“偏小”或“不受影响”)。

| A的质量/ g | S的质量/ g | AS的质量/ g | |
| 甲 | 8 | 4 | 11 |
| 乙 | 7 | 5 | 11 |
| 丙 | a | b | 6.6 |

下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| A.物质:CO2;所含杂质:O2;除去杂质的方法:通过灼热的铜网 |
| B.物质:KOH溶液;所含杂质:K2CO3;除去杂质的方法:加入足量稀盐酸至不再产生气泡 |
| C.物质:NaC |
| D.物质:H2;所含杂质:H2O;除去杂质的方法:通过浓H2SO4 |
小李在化学实验技能考查中,完成“用稀盐酸鉴别氢氧化钠溶液
 和碳酸钠溶液,并测碳酸钠溶液的pH”实验。
和碳酸钠溶液,并测碳酸钠溶液的pH”实验。
【实验一】小李取待测液甲、乙分别放置在试管①和②,再往两支试管中
滴入稀盐酸,观察实验现象。根据现象推知,乙为碳酸钠溶液。
(1)实验中,小李应观察到试管②的现象是__________________________________,
该试管中反应的化学方程式为_________________________________。
(2)老师指出:除盐酸外,还可使用其它试剂鉴别氢氧化钠和碳酸钠溶液。请你选择一
种不属于酸的试剂,并将鉴别实验中的预期现象以及化学方程式填入下表。
| 选择的试剂 | 预期现象 | 反应的化学方程式 |
| ____________ | 一支试管无明显现象; 另一支试管________________ | _________________________ |
【实验二】小李用玻璃棒蘸取“实验一”后试管②中的溶液沾在pH试纸上,观察试纸颜
色变化并与标准比色卡对照,读出溶液的pH。小李的记录如下:
| 实验现象 | 结论 |
| 溶液沾在试纸上时,试纸缓慢地变色 | 与标准比色卡对比,Na2CO3溶液pH=3 |
(3)小李因操作错误,得出“Na2CO3溶液pH=3”的错误结论。指出小李操作错误之处。
答:_______________________________________________________________。
(4)指出小李记录的“实验现象”中不科学的地方。
答:_______________________________________________。
 l;所含杂质:CaCO3;除去杂质的方法:溶解、过滤、蒸发
l;所含杂质:CaCO3;除去杂质的方法:溶解、过滤、蒸发