��Ŀ����
��ѧ��ȤС���ͬѧΪ�˲ⶨij������ʯ��������������������
��.��ͬѧȡһ�������ij�������������ľ̿�ۻ�Ϻ�����ͼ��ʾװ���Ժ����IJ�������ⶨ����������ʼ�ղ������仯����
��.��ͬѧȡһ�������ij�������������ľ̿�ۻ�Ϻ�����ͼ��ʾװ���Ժ����IJ�������ⶨ����������ʼ�ղ������仯����

�� ʵ���г���ͨ�����ĵ���������ǰ����ͨ��һ��ʱ�䣬��������_________________
�� ��Ӧ������ͬѧϨ������ƵĻ��������ֹͣͨ��N2�����IJ�������_________ ˵������_______________
���������������Һ�������ģ��Զ�����̼����������ȫ�ģ���ô��ͬѧ������������Һ�����زⶨ��������������������___________(ѡ�ƫ����ƫС����ȷ��)��ԭ����____________�����������С���ĸĽ���ʩ��__________________��
����ͬѧȡ��ʯ��Ʒ10g����������ϡ���ᣬ��ȫ��Ӧ����ȥϡ����112.5g�����˵õ�����2.5g (�������ʼȲ�����ˮҲ�����ᷢ����Ӧ)���������ͬѧ������������ʯ�������������������ͷ�Ӧ����Һ���Ȼ�������������������������б�����λС�������ȷ��0.1%��
�� ��Ӧ������ͬѧϨ������ƵĻ��������ֹͣͨ��N2�����IJ�������_________ ˵������_______________
���������������Һ�������ģ��Զ�����̼����������ȫ�ģ���ô��ͬѧ������������Һ�����زⶨ��������������������___________(ѡ�ƫ����ƫС����ȷ��)��ԭ����____________�����������С���ĸĽ���ʩ��__________________��
����ͬѧȡ��ʯ��Ʒ10g����������ϡ���ᣬ��ȫ��Ӧ����ȥϡ����112.5g�����˵õ�����2.5g (�������ʼȲ�����ˮҲ�����ᷢ����Ӧ)���������ͬѧ������������ʯ�������������������ͷ�Ӧ����Һ���Ȼ�������������������������б�����λС�������ȷ��0.1%��
�ٽ�װ���ڵĿ����ž�
�ڲ��ԣ�b �е�NaOH ��Һ�ᵹ����a �����Ӳ�ʲ���������
��ƫС�� �����������ص�������һ����̼�����ɺ�������ߵ�ˮ������ƫС����ab ֮������һ��ʢ������ͭ����ͷͨ�IJ����ܺ�a װ��ͬʱ���ȣ���b ����һ������װ�ú�b һ������ء�
��. ����ʯ����������=(10g-2.5g)/10g ��100%=75%
���7.5g Fe2O3��Ӧ����FeCl3����Ϊx ��
Fe2O3 + 6HCl === 2FeCl3 + 3H2O
160 ������325
��7.5g ������ x
160:325=7.5g:X �� X=15.23g
��Һ��FeCl3����������=15.23g/(7.5g+112.5g) ��100% =12.7%
�ڲ��ԣ�b �е�NaOH ��Һ�ᵹ����a �����Ӳ�ʲ���������
��ƫС�� �����������ص�������һ����̼�����ɺ�������ߵ�ˮ������ƫС����ab ֮������һ��ʢ������ͭ����ͷͨ�IJ����ܺ�a װ��ͬʱ���ȣ���b ����һ������װ�ú�b һ������ء�
��. ����ʯ����������=(10g-2.5g)/10g ��100%=75%
���7.5g Fe2O3��Ӧ����FeCl3����Ϊx ��
Fe2O3 + 6HCl === 2FeCl3 + 3H2O
160 ������325
��7.5g ������ x
160:325=7.5g:X �� X=15.23g
��Һ��FeCl3����������=15.23g/(7.5g+112.5g) ��100% =12.7%

��ϰ��ϵ�д�
�����Ŀ
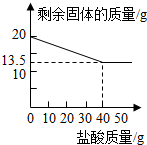 ij��ѧ��ȤС���ͬѧΪ�ⶨ�ٻƽ�ͭп�Ͻ����Ԫ�ص�������������ȡ20�˼ٻƽ������ձ��У���ijŨ�ȵ�ϡ����50�ˣ���5�μ��룬ÿ�γ�ַ�Ӧ��ȡ�����壬�����ˡ�����Ȳ����������5��ϡ����������ʣ�����������¼���£�
ij��ѧ��ȤС���ͬѧΪ�ⶨ�ٻƽ�ͭп�Ͻ����Ԫ�ص�������������ȡ20�˼ٻƽ������ձ��У���ijŨ�ȵ�ϡ����50�ˣ���5�μ��룬ÿ�γ�ַ�Ӧ��ȡ�����壬�����ˡ�����Ȳ����������5��ϡ����������ʣ�����������¼���£�| ʵ����� | ϡ�����������g�� | ʣ������������g�� |
| 1 | 10 | 18.375 |
| 2 | 10 | 16.750 |
| 3 | 10 | 15.125 |
| 4 | 10 | 13.500 |
| 5 | 10 | 13.500 |
��2������ϡ���������ʵ�����������
��3�����Ͻ��е�п��ϡ����ǡ����ȫ��Ӧʱ��������Һ�����ʵ���������Ϊ���٣�
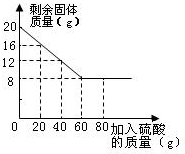 ij��ѧ��ȤС���ͬѧΪ�ⶨCu��CuO�����Ʒ��CuO�ĺ������ס��ҡ���������λͬѧ���ȳ�ȡ20g��Ʒ���ձ��У��ڷֱ����20g��40g��60g��80g��������������ͬ��ϡ���ᣮ��ַ�Ӧ���й���ʣ�࣮�����ˡ�����������ʣ�������������ͼ��ʾ���ش��������⣺
ij��ѧ��ȤС���ͬѧΪ�ⶨCu��CuO�����Ʒ��CuO�ĺ������ס��ҡ���������λͬѧ���ȳ�ȡ20g��Ʒ���ձ��У��ڷֱ����20g��40g��60g��80g��������������ͬ��ϡ���ᣮ��ַ�Ӧ���й���ʣ�࣮�����ˡ�����������ʣ�������������ͼ��ʾ���ش��������⣺