题目内容
17.关于物质的用途,下列说法不合理的是( )| A. | 稀盐酸用于除铁锈 | B. | 氢氧化铝用于治疗胃酸过多 | ||
| C. | 浓硫酸在实验室中常用作干燥剂 | D. | 氢氧化钠固体可用于干燥CO2 |
分析 A、根据稀盐酸可与金属氧化物反应进行解答;
B、根据氢氧化铝可与稀盐酸反应进行解答;
C、根据浓硫酸具有吸水性进行解答;
D、根据氢氧化钠可以和二氧化碳反应进行解答.
解答 解:
A、稀盐酸可与金属氧化物反应,铁锈的主要成分是氧化铁,故可用于除铁锈,故A正确;
B、胃酸的成分是盐酸,Al(OH)3属于碱类,能够和人体胃中过多的胃酸中的主要成分盐酸反应生成氯化铝和水,故B正确;
C、浓硫酸具有吸水性,在实验室中常用作干燥剂,故C正确;
D、氢氧化钠固体具有吸水性,可以和二氧化碳反应,不能用于干燥CO2,故D错误.
故选D.
点评 物质的性质决定用途,用途又反映了物质的性质,根据物质的性质细心分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列有关分子、原子和离子的叙述中,正确的是( )
| A. | 氯原子得到1个电子形成带负电荷的氯离子 | |
| B. | 原子是由质子和中子构成的 | |
| C. | 分子的质量总比原子的质量大 | |
| D. | 保持水的化学性质的粒子是氢原子和氧原子 |
5.下列物质属于纯净物的是( )
| A. | “蒙牛”加钙纯牛奶 | B. | “花冈岩”岩石 | ||
| C. | 洁净的空气 | D. | 蒸馏水 |
12.写出下列你熟悉物质的符号(请注意大小写的区分)
| 物质名称 | 水 | 氧气 | 二氧化碳 | 铜片 | 镁条 | 氧化铜 |
| 化学符号 |
9.2015年3月28日是本年度的“地球一小时”(Earth Hour)活动日,为响应全球应对气候变化主题,今年“地球一小时”在中国将继续聚焦当前最急迫、最受关注的环境议题--雾霾,发出“能见蔚蓝”的倡议.下列做法不符合这一主题的是( )
| A. | 汽车限购限行 | B. | 采用焚烧的方法处理农作物的秸秆 | ||
| C. | 广泛使用太阳能和风能等清洁能源 | D. | 禁止燃放烟花炮竹 |
6. 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验装备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO5、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
表中的现象Ⅰ为有气泡产生;现象Ⅱ对应反应的化学方程式为Ca(OH)2+Na2CO3=2NaOH+CaCO3↓;
(2)实验过程
[实验1]证明反应生成了Na2CO3
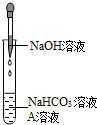
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2溶液;
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有;
[实验2]证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有;
(3)实验反思:
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.(1)实验装备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO5、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)实验过程
[实验1]证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2溶液;
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有;
[实验2]证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有;
(3)实验反思:
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.