题目内容
请依据下列信息回答有关问题:Cl2是一种黄绿色、具有刺激性气味、有毒的气体,其密度比空气的密度大.能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水.Cl2可用于消毒饮用水等.在实验室里常用下述反应制取氯气:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑

(1)写出氯气与氢氧化钠溶液反应的化学方程式: ;生成物中氯元素的化合价分别为 .
(2)实验室选择气体发生装置应考虑的因素有 和 .
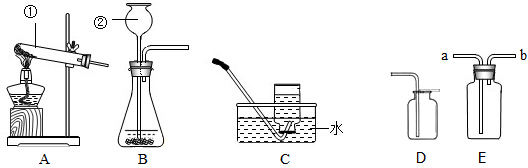
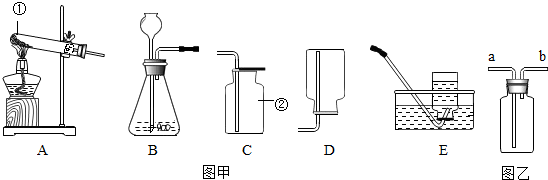
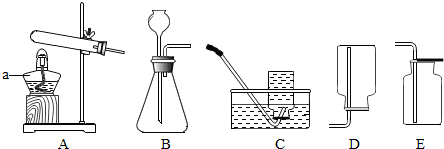
(3)如图,在实验室里制取氯气应选择的发生装置是 (填字母);收集氯气选用D装置,请推测其中氢氧化钠溶液的作用是 .
(4)如图,若选用B、E组合在实验室可制取 气体,反应方程式为 .
(5)12.5g大理石与稀盐酸完全反应后,可生成二氧化碳气体4.4g,请计算大理石中杂质的质量分数.
| ||

(1)写出氯气与氢氧化钠溶液反应的化学方程式:
(2)实验室选择气体发生装置应考虑的因素有
(3)如图,在实验室里制取氯气应选择的发生装置是
(4)如图,若选用B、E组合在实验室可制取
(5)12.5g大理石与稀盐酸完全反应后,可生成二氧化碳气体4.4g,请计算大理石中杂质的质量分数.
考点:常用气体的发生装置和收集装置与选取方法,实验室制取气体的思路,气体的净化(除杂),有关元素化合价的计算,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:常见气体的实验室制法、检验、干燥与净化
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.D装置中氢氧化钠溶液的作用是:吸收多余的氯气,防止污染空气.
解答:解:(1)氯气能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水,配平即可;生成物中氯元素的化合价分别为:NaCl中-1价,NaClO中+1价;故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;-1价、+1价;
(2)气体的制取装置的选择与反应物的状态和反应的条件有关,故答案为:反应物的状态;反应的条件;
(3)D装置中氢氧化钠溶液的作用是:吸收多余的氯气,防止污染空气;故答案为:B;吸收多余的氯气,防止污染空气;
(4)如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;故答案为:氧气或氢气;2H2O2
2H2O+O2↑或Zn+H2SO4=ZnSO4+H2↑;
(5)设大理石中碳酸钙的质量分数为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
12.5g?x 4.4g
=
x=80% 因此大理石中杂质的质量分数=1-80%=20%;
答:大理石中杂质的质量分数20%;
故答案为:20%
(2)气体的制取装置的选择与反应物的状态和反应的条件有关,故答案为:反应物的状态;反应的条件;
(3)D装置中氢氧化钠溶液的作用是:吸收多余的氯气,防止污染空气;故答案为:B;吸收多余的氯气,防止污染空气;
(4)如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;故答案为:氧气或氢气;2H2O2
| ||
(5)设大理石中碳酸钙的质量分数为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
12.5g?x 4.4g
| 100 |
| 44 |
| 12.5g?x |
| 4.4g |
答:大理石中杂质的质量分数20%;
故答案为:20%
点评:本考点主要考查了元素的化合价、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目


 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004.牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签上的部分文字.请仔细阅读后回答下列问题:
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其相对分子质量为1004.牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签上的部分文字.请仔细阅读后回答下列问题: