题目内容
关于硫酸的下列叙述中正确的是( )
| A、稀释浓硫酸时,一定要把水倒入浓硫酸中及时搅拌 |
| B、由于硫酸不具有挥发性,故实验室制备CO2时用硫酸比盐酸好 |
| C、判断未知溶液是否是硫酸,可将氯化钡溶液滴入,观察是否有白色沉淀,有则是硫酸 |
| D、硫酸溶液具有导电性,是因为硫酸在水中能电离产生阳离子和阴离子 |
考点:酸的化学性质,浓硫酸的性质及浓硫酸的稀释,溶液的导电性及其原理分析
专题:常见的酸 酸的通性
分析:A、据稀释浓硫酸的方法分析解答;
B、据硫酸和碳酸钙反应生成的硫酸钙的性质回答;
C、据硫酸根离子的检验方法分析解答;
D、据溶液导电原因分析解答.
B、据硫酸和碳酸钙反应生成的硫酸钙的性质回答;
C、据硫酸根离子的检验方法分析解答;
D、据溶液导电原因分析解答.
解答:解:A、浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌;切不可将水倒进浓硫酸里,故错误;
B、硫酸和碳酸钙反应生成微溶的硫酸钙,会覆盖在碳酸钙表面,阻止反应的进行,所以不能用硫酸制取,故错误;
C、判断未知溶液是否是硫酸,将氯化钡溶液滴入,生成的沉淀可能为AgCl、硫酸钡沉淀,所以不能确定是否一定含有SO42-,应先加盐酸酸化,如无沉淀再加入氯化钡观察,故错误;
D、硫酸溶液具有导电性,是因为硫酸在水中电离产生自由移动的氢离子和硫酸根离子,正确;
故选:D.
B、硫酸和碳酸钙反应生成微溶的硫酸钙,会覆盖在碳酸钙表面,阻止反应的进行,所以不能用硫酸制取,故错误;
C、判断未知溶液是否是硫酸,将氯化钡溶液滴入,生成的沉淀可能为AgCl、硫酸钡沉淀,所以不能确定是否一定含有SO42-,应先加盐酸酸化,如无沉淀再加入氯化钡观察,故错误;
D、硫酸溶液具有导电性,是因为硫酸在水中电离产生自由移动的氢离子和硫酸根离子,正确;
故选:D.
点评:了解硫酸的性质,硫酸根离子的检验等知识,才能灵活分析解答相关问题.

练习册系列答案
相关题目
下列描述的物质的物理性质的是( )
| A、可燃性 | B、导电性 |
| C、毒性 | D、腐蚀性 |
下列化学方程式表示的反应,符合实验事实的是( )
| A、Cu+2HCl═CuCl2+H2↑ |
| B、2KNO3+MgCl2═Mg(NO3)2+2KCl |
| C、CuSO4+Zn═ZnSO4+Cu |
| D、2Fe+3H2SO4═Fe2(SO4)3+3H2↑ |
下列物质的俗名与化学式一致的是( )
| A、水银Ag |
| B、纯碱NaHCO3 |
| C、酒精CH3OH |
| D、烧碱NaOH |
下列物质不属于合金的是( )
| A、青铜 | B、不锈钢 | C、钢 | D、氧化铁 |
将市场上的蔬菜用塑料袋装好,放了一晚上后,将袋中的气体通入澄清石灰水,发现石灰水变浑浊,这说明( )
| A、植物发生了光合作用放出了二氧化碳 |
| B、植物发生了呼吸作用放出了二氧化碳 |
| C、植物发生了光合作用放出了氧气 |
| D、植物发生了呼吸作用放出了氧气 |
在称取13.4g 食盐时,误将13g 砝码放在左托盘,食盐放在右托盘,则实际称得食盐的质量应为( )
| A、12.6 g |
| B、13 g |
| C、13.4 g |
| D、13.8 g |
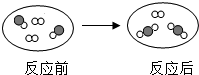 如图为某化学反应的微观示意图,其中“
如图为某化学反应的微观示意图,其中“ ”和“
”和“ ”表示不同元素的原子.下列说法错误的是( )
”表示不同元素的原子.下列说法错误的是( )| A、生成物是化合物 |
| B、化学反应前后原子个数不变 |
| C、生成物的每个分子由三个原子构成 |
D、参加反应的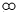 和 和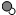 的个数比为1:1 的个数比为1:1 |